Zoledronato para la prevención de la pérdida ósea en mujeres que suspenden el tratamiento con denosumab
5 de febrero 2020
Zoledronate for the Prevention of Bone Loss in Women Discontinuing Denosumab Treatment. A Prospective 2-Year Clinical Trial. Anastasilakis AD, Papapoulos SE, Polyzos SA, et. al. J Bone Miner Res. 2019 Dec;34(12):2220-2228. doi: 10.1002/jbmr.3853.
Este artículo está protegido por derechos de autor
Introducción
La interrupción del tratamiento con denosumab (Dmab) se asocia con aumentos en el recambio óseo por encima de los valores basales y una pérdida ósea rápida.
En este estudio se investigó la eficacia del zoledronato (ZOL) para prevenir esta pérdida ósea en mujeres con osteoporosis posmenopáusica que fueron tratadas con Dmab (duración media de 2.2 años) y descontinuaron el tratamiento después de lograr osteopenia.
Diseño del estudio
Las mujeres fueron aleatorizadas para recibir una sola infusión de 5 mg de ZOL (n = 27) o dos inyecciones adicionales de 60 mg de Dmab (n = 30), seguidos por un total de 24 meses. Fig1.
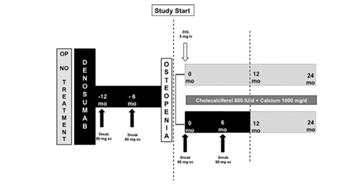
Fig 1. Diseño del estudio. Los cuadros negros indican el tratamiento con Dmab.
ZOL = zoledronato; Dmab = denosumab; i.v. = intravenoso; s.c. subcutaneo = subcutáneo; mo = meses; OP = osteoporosis.
Objetivos de estudio
El endpoint primario: diferencia del cambio en la DMO en columna lumbar (CL) entre los dos grupos de 12 a 24 meses.
Los endpoints secundarios: diferencia en los cambios de la DMO del cuello femoral (CF) entre los dos grupos de 12 a 24 meses; la diferencia de cambio en la DMO de CL y CF entre los dos grupos en 12 meses; las diferencias en los marcadores de recambio óseo entre los dos grupos a lo largo del estudio y la relación entre marcadores séricos y cambios en la DMO.
Entre los endpoints exploratorios se evaluó la incidencia de nuevas fracturas vertebrales (clínicas y morfométricas) y otras fracturas por fragilidad.
Resultados
57 mujeres fueron asignados aleatoriamente (1:1) para continuar Dmab (n 30) o recibir
ZOL (n 27). La infusión de ZOL fue administrada a los 6.5 ±0.1 meses después de la última inyección de Dmab. Ver características basales en tabla.
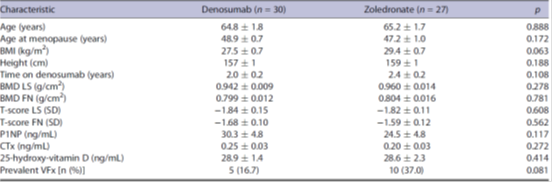 Tabla. Características clínicas, radiológicas y bioquímicas basales
Tabla. Características clínicas, radiológicas y bioquímicas basales
Los datos se presentan como media ± DE. DMO = densidad mineral ósea; IMC = índice de masa corporal; CTX = telopéptido C-terminal de colágeno tipo 1; FN = cuello femoral; LS = columna lumbar; P1NP = propéptido procolágeno tipo 1 N-terminal; VFx = fracturas vertebrales.
DMO
En comparación con la línea de base, la DMO de CL aumentó, pero no significativamente, en ambos grupos a los 12 meses (ZOL 1.7 ±1.1%, p=0.384; Dmab 2.1 ±1.0%, p=0.150). A los 24 meses, la DMO en CL volvió a la línea de base en el grupo ZOL (en comparación con la línea de base: 0.1 ±1.2%; p=0.203), pero disminuyó significativamente en el grupo Dmab en del valor de 12 meses (-4.82 ± 0.7%; p<0.001), alcanzando valores que también fueron significativamente más bajos que el basal (p=0.021).
La diferencia en la DMO en CL entre los dos grupos del mes 12 al 24, endpoint primario, fue significativa (p=0.025), al igual que la diferencia en cambios en la DMO de CF (p=0.005) (Fig. 2).
Las diferencias en los cambios de DMO entre los dos grupos, 24 y 12 meses después de la interrupción de Dmab (6 meses después la última inyección) para el grupo ZOL y Dmab, respectivamente, también fueron estadísticamente significativos tanto en la DMO de CL (p=0.003) como en CF (p=0.007).
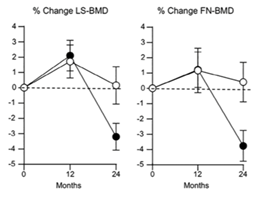
Fig 2. Cambios porcentuales (promedioï±DE) en DMO columna lumbar (izquierda) y cuello femoral (derecha) desde el inicio en mujeres tratadas con ZOL (círculos abiertos) y Dmab (círculos cerrados).
Marcadores de recambio óseo
La infusión de ZOL fue seguida por un pequeño pero significativo aumento de CTX y P1NP durante el primer año, con estabilización posterior. A los 24 meses, los niveles séricos de P1NP estaban por encima del límite superior de los valores normales para posmenopausia en dos pacientes (7,4%) y en otras cinco pacientes estos estaban por encima del rango de referencia de la premenopausica. Una sola infusión de ZOL, aunque altamente eficaz, no pudo retener completamente los niveles de los marcadores dentro del rango de referencia (ya sea premenopausica o posmenopáusica) después de la interrupción de Dmab más de 2 años.
En pacientes tratados con Dmab, no hubo cambio en los valores medios de ambos marcadores durante los primeros 12 meses y ningún paciente tenía valores séricos por encima del límite superior del rango de referencia. Al mes 15 (9 meses después de la última inyección de Dmab) los valores de P1NP y CTX en suero aumentaron significativamente, alcanzando niveles que también fueron significativamente más altos que los del grupo ZOL. A los 24 meses solo dos pacientes tenían valores de P1NP dentro del rango premenopáusico.
Por lo tanto, independientemente de la definición del rango de referencia, altos niveles de los marcadores óseos persistieron 18 meses después de la última inyección de Dmab en la mayoría de los pacientes estudiados.
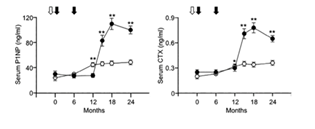
Fig 3. Valores de P1NP sérico (izquierda) y CTX (derecha) durante el estudio. Círculos cerrados = Dmab; círculos abiertos = ZOL; flecha abierta = ZOL 5 mg i.v .; flechas cerradas = Dmab 60 mg s.c.
* Significativamente diferente de la línea de base. ** Significativamente diferente de la línea de base y entre grupos.
Relación entre los valores de los marcadores óseos séricos y los cambios en la DMO
No hubo asociación entre los valores de los marcadores óseos, tanto basales como a los 12 meses, con los cambios en la DMO en ambos grupos durante todo el estudio.
Particularmente importante para la práctica clínica fue la falta de relación en mujeres tratadas con ZOL; incluso cuando se dividieron de acuerdo a el valor medio basal (por debajo o por encima del mismo) no hubo diferencia significativa en los cambios en la DMO a los 12 o 24 meses entre los dos subgrupos (valores de p entre 0.1 y 0.895 para todas las mediciones de DMO tanto para P1NP como CTX).
También se evaluaron los cambios individuales en la DMO de CL (12 a 24 meses) por arriba o por debajo del mínimo cambio significativo, en mujeres tratadas con Dmab, y no hubo diferencias significativas en la edad, número de inyecciones de Dmab y valores de los marcadores óseos entre pacientes con pérdida ósea â¥5% en comparación con aquellas con pérdida ósea <5%.
Los resultados de estos análisis combinados indican que los cambios de la DMO luego de una infusión de ZOL o de la interrupción de Dmab, no pueden ser predichos por los marcadores óseos o cualquiera de las características clínicas evaluadas.
Fracturas
Durante el estudio, tres pacientes sufrieron fracturas vertebrales clínicas y no hubo fracturas no vertebrales.
⢠Grupo ZOL: 1 paciente (3.7%) tuvo una nueva fractura vertebral y empeoramiento de una deformidad vertebral preexistente, 12 meses después de la infusión de ZOL (18 meses después del último Dmab). Se asociaron con profunda pérdida de DMO CF a los 12 meses, y no se relacionaron con aumento en los marcadores óseos, inmovilización, u enfermedad subyacente.
⢠Grupo Dmab: 2 pacientes (6,7%) tuvieron en una nueva fractura vertebral y empeoramiento de 2 fracturas prevalentes en el primer paciente, y una nueva y un empeoramiento en el segundo paciente, a los 9 y 12 meses después de la última inyección de Dmab. En un paciente asintomático con una fractura vertebral prevalente, una nueva fractura vertebral morfométrica fue observada en radiografía a los 24 meses.
Eventos adversos
18 (66.7%) de las 27 mujeres en el grupo ZOL desarrollaron síntomas compatibles con una reacción de fase aguda transitoria. No se registraron eventos adversos en el grupo Dmab. No hubo casos de osteonecrosis de mandíbula ni fractura femoral atípica.
Discusión
Aunque aún se sigue en debate, en general uno de los objetivos específicos del tratamiento con denosumab es el logro de valores de DMO en rango no osteoporótico.
En el estudio de la FREEDOM y su extensión, se demostró que Dmab aumenta la DMO a tales niveles en un número sustancial de mujeres con osteoporosis posmenopáusica que podría conducir en la práctica clínica a la interrupción del tratamiento cuando se alcanza dicho objetivo. Sin embargo, el efecto de Dmab, es rápidamente reversible, y puede asociarse en algunos pacientes con una mayor incidencia de fracturas vertebrales clínicas. Por lo que se necesita una estrategia para consolidar y mantener las ganancias en la DMO por períodos más prolongados.
En este trabajo se muestra como una solo infusión de 5 mg i.v. de ZOL, 6 meses después de la última inyección de Dmab, mantiene la DMO en la columna lumbar y en la cadera en mujeres con DMO en rango de osteopenia durante 1 año, y en la mayoría de ellas durante 2 años.
La eficacia de ZOL para preservar las ganancias de DMO luego de Dmab se examinó previamente en series de casos, donde las respuestas a ZOL fueron variables con pequeñas pérdidas de DMO hasta la reversión completa de la ganancia obtenida con Dmab.
La eficacia de los bisfosfonatos orales para prevenir la pérdida ósea después de Dmab también fue evaluada en distintos estudios con resultados variables. Aunque actualmente se recomienda continuar el tratamiento de pacientes que suspenden Dmab con agentes antirresortivos, la evidencia que respalda esta recomendación no es robusta.
A estas diferencias reportadas en los distintos estudios pueden contribuir, la duración del tratamiento con Dmab, otros tratamientos previos, DMO basal, así como el tiempo de administración de ZOL después de la última inyección de Dmab.
Este estudio, además de mostrar la eficacia de ZOL en la prevención de la pérdida ósea después de la interrupción de Dmab en mujeres con osteopenia posmenopáusica, permite la evaluación prospectiva de moduladores en la respuesta a este bisfosfonato.
El pensamiento convencional y estudios con agentes antirresortivos han mostrado mayores incrementos en la DMO en pacientes con mayores tasas de recambio óseo, lo que respalda la noción de que ZOL podría tener un mejor efecto sobre la DMO si el remodelado no está disminuido. En línea con estas consideraciones, Horne y colegas sugirieron que retrasar la administración de ZOL durante la transición de Dmab, por más de 6 meses puede aumentar la extensión de mantenimiento de la ganancia en la DMO, una sugerencia también apoyada por datos limitados obtenidos en el período de observación de 4 años del estudio DATA.
Estos argumentos pueden afectar la práctica clínica porque podría conducir a elecciones arbitrarias del momento de la administración de ZOL o en tener que realizar mediciones repetidas de los marcadores hasta el aumento de los mismos.
En este estudio se muestra que la variabilidad de los cambios en la DMO después del ZOL no está relacionada con la tasa de recambio óseo en el momento de la infusión o en cualquier otro momento evaluado durante el tratamiento. Esto sugiere por lo tanto, que no hay razón para retrasar la administración de ZOL más allá 6 meses después de la última inyección de Dmab. Tampoco se encontró asociación entre las respuestas de la DMO y el número de inyecciones de Dmab en ambos grupos de pacientes.
Sin embargo, en este trabajo se observó una variabilidad significativa en la respuesta de la DMO individual a ZOL especialmente a los 2 años, cuando tres de 27 pacientes tuvieron disminuciones en la DMO de CL superior al mínimo cambio significativo que no pudo explicarse por el momento de la infusión, la tasa de recambio óseo basal o la DMO basal.
Por lo tanto, en la práctica clínica, es aconsejable medir la DMO a los 12 meses después de la infusión de ZOL y decidir si requieren tratamiento adicional algunos pacientes.
Este trabajo, también brindó la oportunidad de comparar por primera vez el efecto de una sola infusión de ZOL 5 mg con Dmab 60 mg s.c. cada 6 meses durante 1 año en pacientes tratados previamente con este último, observando mayores incrementos en DMO de CL con Dmab en comparación con ZOL pero que no fueron estadísticamente significativos.
El aumento observado en los marcadores óseos, después de la interrupción de Dmab sin ningún tratamiento posterior, fue similar a lo ya descripto. Sin embargo, este aumento no se asoció con los cambios en la DMO en ambos grupos de pacientes. En un número considerable de mujeres en el grupo Dmab, los marcadores todavía estaban por encima del límite superior de la normalidad del rango para la posmenopausia, 18 meses después de la última inyección de Dmab pero también en 7.4% de pacientes tratados con ZOL a los 2 años. En este último grupo, no se sabe si los marcadores ya estaban altos antes de iniciar Dmab, o si se deben a un efecto prolongado de la suspensión de Dmab que no se pudo prevenir con ZOL, porque los datos previos al tratamiento no estaban disponibles.
La incidencia de todas las fracturas vertebrales después de la interrupción de tratamiento en el grupo Dmab fue del 10% y el de múltiples fracturas vertebrales clínicas fue del 6,7%. A pesar del pequeño número de pacientes estudiados prospectivamente, esta incidencia es similar a lo observado durante 1 año de seguimiento observacional de 65 mujeres tratadas con Dmab en un estudio de fase 2 (7.7%), por McClung y col.
Estos resultados junto con los del análisis post hoc del estudio FREEDOM y su extensión, indican que la frecuencia de este evento es baja, como también se informó recientemente en una gran serie retrospectiva.
Hay muchos reportes con bajo número de pacientes y diferentes diseños, con distintos resultados, que no permiten comparar entre estudios y confirmar o refutar un vínculo causal con el tratamiento previo con Dmab, como en el paciente del trabajo actual que tuvo un empeoramiento de una deformidad vertebral preexistente y una nueva fractura 12 meses después de la administración de ZOL.
Es importante destacar que los cuatro pacientes con fracturas vertebrales (tres clínicas, una morfométrica) tenían fracturas vertebrales prevalentes previas.
Las fracturas vertebrales prevalentes han sido reportadas previamente como el factor de riesgo más importante para fracturas vertebrales clínicas después de la interrupción de Dmab. Esto sugiere fuertemente que se deben realizar radiografías de la columna en todos los pacientes en quienes se considere la interrupción del tratamiento.
Las limitaciones de este trabajo incluyen la pequeña cantidad de mujeres tratados, el diseño de etiqueta abierta y la duración de tratamiento con Dmab relativamente corta.
Sin embargo, esta duración del tratamiento es consistente con los hallazgos del "mundo real" que muestran la adherencia al tratamiento con Dmab durante 2 años en aproximadamente
50% de los pacientes en la mayoría de los estudios. El beneficio del número relativamente pequeño de los pacientes, es que permitió el análisis detallado de respuestas individuales, generalmente no disponibles en ensayos grandes, que proporcionaron información importante para la atención clínica.
En conclusión, en la mayoría de las mujeres con osteoporosis posmenopáusica tratadas con Dmab en quienes la interrupción del tratamiento es considerada cuando se logra osteopenia densitométrica, una sola infusión de ZOL 5 mg administrada 6 meses después de la última inyección de Dmab evita la pérdida ósea durante al menos 2 años independientemente de la tasa de recambio óseo. Se recomienda seguimiento, porque en algunos pacientes el tratamiento podría no tener el esperado efecto a los 2 años por razones actualmente desconocidas.
Copyrigth2020 ENDOweb. Citar este artículo: Zoledronato para la prevención de la pérdida ósea en mujeres que suspenden el tratamiento con denosumab – 5 de febrero 2020

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!