Tratamiento con Romosozumab en mujeres posmenopáusicas con Osteoporosis
17 de noviembre 2016
Romosozumab Treatment in Postmenopausal Women with Osteoporosis. Cosman F, Crittenden DB, Adachi JD, Binkley N, Czerwinski E, Ferrari S, et. al. N Engl J Med. 2016 Oct 20;375(16):1532-1543.
El descubrimiento de que la deficiencia de esclerostina causa condiciones genéticas raras que se caracterizan por una masa ósea elevada y mayor resistencia a las fracturas, la convirtió en un blanco terapéutico para la osteoporosis.
La esclerostina, secretada por los osteocitos, es un regulador negativo de la formación de hueso. Inhibe la señalización de la vía Wnt, regulando negativamente el desarrollo de osteoblastos y su función.
El Romosozumab (Romo) es un anticuerpo monoclonal que se une a la esclerostina y la inhibe, con un doble efecto: aumenta la formación y disminuye la resorción de hueso.
El tratamiento con Romo en dosis de 210mg mensual subcutáneo durante un año, en mujeres posmenopáusicas con baja masa ósea (ensayo clínico fase 2), mostró un aumento significativo de la densidad mineral ósea (DMO), de los marcadores de formación durante los primeros 6 a 9 meses de tratamiento, y disminución persistente de los marcadores de resorción ósea.
En base a estos resultados se realizó el ensayo clínico de fase 3, que evaluó los efectos de Romo en el riesgo de fracturas, durante un año de tratamiento en mujeres con osteoporosis posmenopáusica. Dada la evidencia de que la DMO se mantiene o puede aumentar después de la transición de un tratamiento con un agente de formación a un agente antiresortivo, también se evaluó el seguimiento de la terapia con Denosumab (Dmab) como tratamiento secuencial para la osteoporosis.
MÃTODOS
Diseño del ensayo
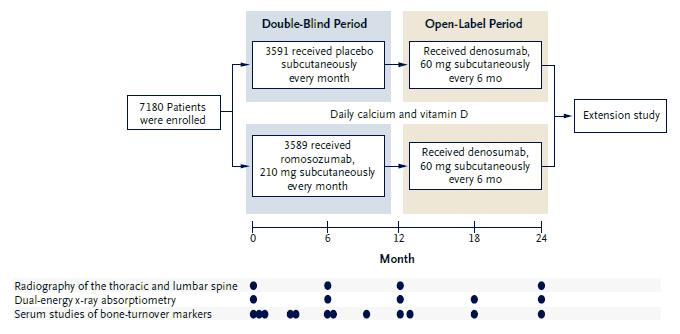
El estudio Fracturas en Mujeres Posmenopáusicas con Osteoporosis (FRAME) fue un estudio internacional, doble ciego, controlado con placebo, randomizado y de grupos paralelos. Las mujeres fueron randomizadas 1:1 a recibir Romo 210 mg o placebo. La aleatorización se estratificó según la edad (<75 años y ⥠75 años) y presencia o ausencia de fracturas vertebrales prevalentes. Romo o placebo se administró por vía subcutánea una vez al mes durante 12 meses, y luego fue seguido de un tratamiento abierto con Dmab 60 mg cada 6 meses por vía subcutánea, durante 12 meses adicionales (Fig. 1).
Pacientes
Se incluyeron mujeres posmenopáusicas ambulatorias, de 55 a 90 años de edad, con un T score en cadera total o cuello femoral entre -2,5 y -3.5, que tuvieran al menos dos vértebras evaluables en la región L1L4 y al menos una de las caderas evaluables por densitometría. Se excluyeron quienes tenían antecedentes de fractura de cadera, cualquier fractura vertebral grave o más de dos fracturas vertebrales moderadas, antecedentes de enfermedad ósea metabólica o condiciones que afecten el metabolismo óseo, osteonecrosis de mandíbula, niveles de 25-hidroxivitamina D menores a 20 ng/ml, hipercalcemia o hipocalcemia actual, o uso reciente de fármacos que afecten el metabolismo óseo. Aquellas pacientes con valores basales de 25-hidroxivitamina D ⤠40 ng/ml, recibieron dosis de carga de 50.000 a 60.000 UI de vitamina D en el momento en que se inició el estudio. Todos los pacientes recibieron calcio (500 a 1000 mg diarios) y vitamina D3 o D2 (600 a 800 UI diarias).
Procedimientos
Se realizaron radiografías laterales de columna vertebral (evaluadas según la clasificación de Genant) en las visitas programadas o si la paciente refería dolor de espalda sugerente de fractura vertebral.
En un sub-estudio que involucró a 128 pacientes, se evaluó la DMO por DXA en columna lumbar y fémur proximal al inicio del estudio y cada 6 meses, y en un sub-estudio en el que participaron 129 pacientes, se determinaron las concentraciones en suero de marcadores de recambio óseo: propéptido del procolágeno tipo 1 N-terminal (P1NP) y el β-isómero de telopéptido del colágeno tipo I C-terminal (β-CTX) (Fig . 1).
Los eventos adversos de interés incluyeron los asociados a la inyección de un anticuerpo monoclonal o a la homeostasis del calcio, y aquellos considerados con potencial relación con hiperostosis. Los anticuerpos anti-romosozumab se evaluaron al inicio y al mes 1, 3, 6, 12, 15 y 24.
Endpoints primarios y secundarios
Los end points primarios fueron la incidencia acumulada de nuevas fracturas vertebrales a los 12 y a los 24 meses.
Los end points secundarios fueron la incidencia acumulada de fracturas clínicas (fracturas no vertebrales y fractura vertebral sintomática), fracturas no vertebrales, fracturas no vertebrales mayores, nueva fractura vertebral o empeoramiento de una preexistente, fractura de cadera, fractura osteoporótica mayor, y múltiples fracturas vertebrales nuevas o que empeoran, a los 12 y a los 24 meses.
RESULTADOS
Pacientes
Fueron randomizadas 7180 pacientes, 6390 (89.0%) completaron 12 meses del ensayo, y 6026 (83.9%) completaron los 24 meses del estudio.
Ambos grupos presentaron similares características demográficas y clínicas basales (Tabla 1). La edad media de las pacientes fue de 70.9 años. El T score medio en columna lumbar fue -2.72, en cadera total de -2.47, y en cuello femoral de -2.75. Un total de 1317 pacientes (18.3%) tenían una fractura vertebral prevalente (la mayoría de las cuales fueron leves), y 1560 (21.7%) tenían una fractura no vertebral previa. Las regiones geográficas con mayor inclusión de pacientes fueron América Latina (3084 pacientes) y Europa central y del este (2093 pacientes).
12 meses de eficacia contra fracturas
El riesgo de nueva fractura vertebral con Romo a 12 meses fue 73% menor que con placebo (incidencia, 0.5% con Romo [16 de 3321) vs. 1.8% placebo [59 de 3322]; razón de riesgo: 0.27; intervalo de confianza del 95% [IC], 0.16 a 0.47; p <0.001) (figura 2A). A los 6 meses, se produjeron nuevas fracturas vertebrales en 14 pacientes con Romo y en 26 con placebo. Entre 6 y 12 meses, las fracturas ocurrieron en 2 pacientes adicionales en el grupo Romo, en comparación con 33 pacientes adicionales en el grupo placebo.
Romo también se asoció con un riesgo 36% menor para fracturas clínicas respecto a placebo a 12 meses; con fracturas en 58 de 3589 pacientes con Romo (1.6%) vs. 90 de 3591 con placebo (2.5%), (razón de riesgo, 0.64; IC del 95%, 0.46 a 0.89; p = 0.008) (Fig. 2B).
Las fracturas no vertebrales constituyeron la mayoría de las fracturas clínicas (> 85%) y se produjeron en 56 pacientes (1.6%) con Romo y en 75 (2.1%) con placebo (razón de riesgo 0.75; IC del 95%, 0.53 a 1.05; p = 0.10) (Figura 2C).
No se observó efecto del tratamiento en las fracturas clínicas y no vertebrales
en todas las regiones geográficas, pero un análisis post hoc mostró que la incidencia de fracturas no vertebrales en la región de América Latina fue del 1.5% (24 de 1550 pacientes) en el grupo Romo frente al 1.2% (19 de 1534) en el grupo placebo (riesgo ratio, 1.25; IC del 95%, 0.68 a 2.27). Por el contrario, entre las pacientes fuera de América Latina, la incidencia fue del 1.6% (32 de 2039) en el grupo Romo frente al 2.7% (56 de 2057) en el grupo placebo, lo que representó un riesgo 42% menor con Romo (razón de riesgo: 0.58; IC 95%, 0.37 a 0.89; p = 0.04 para la interacción tratamiento por región). El riesgo basal para fractura osteoporótica mayor a 10 años según FRAX fue del 8.7% en América Latina y 17% en otros lugares.
24 meses de eficacia contra fracturas
Todos los pacientes realizaron la transición a Dmab en el segundo año. La incidencia acumulada a 24 meses de nuevas fracturas vertebrales fue menor en el grupo que había recibido Romo (21 de 3325 pacientes [0.6%]) comparado con el grupo placebo (84 de 3327 [2.5%]) , con un riesgo 75% menor en el grupo romo (razón de riesgo: 0.25; IC del 95%, 0.16 a 0.40; p <0.001) (Fig. 2A). En el segundo año, 5 pacientes en el grupo que recibió Romo y 25 en el grupo placebo tuvieron una nueva fractura vertebral. No hubo diferencia significativa en el riesgo de fractura no vertebral ni en el riesgo de fractura clínica a los 24 meses (Fig 2B).
Densidad mineral ósea y marcadores de recambio óseo
Romo aumentó la DMO a los 6 meses, y a los 12 meses el porcentaje de cambio respecto al valor basal fue mayor con Romo que con placebo: 13.3 % en columna lumbar (IC del 95%, 11.9 a 14.7), 6.9 % en cadera total (IC del 95%, 5.6 a 8.1), y 5.9% en cuello femoral (IC del 95%, 4.3 a 7.4) (p<0.001 para todas las comparaciones) (Fig . 3A, 3B y 3C). La DMO continuó aumentando en el grupo Romo después de la transición a Dmab (p<0.001 para todas las comparaciones entre los grupos que recibieron originalmente Romo vs. placebo) (Fig. 3A, 3B y 3C).
Los niveles del marcador de formación P1NP aumentaron rápidamente en el grupo de Romo (máximo en el día 14) y volvieron a los niveles basales por 9 meses. Los niveles del marcador de resorción óseaβ-CTX disminuyeron en forma temprana (máximo descenso en el día 14) y se mantuvieron por debajo de los niveles del grupo placebo a los 12 meses (Fig. 3D y 3E). A los 14 días de la administración de Romo o placebo se observaron aumentos transitorios de P1NP y disminución de β-CTX en el grupo Romo. El tratamiento con Dmab redujo los niveles de P1NP y β -CTX de manera similar en cada grupo.
Eventos adversos y seguridad
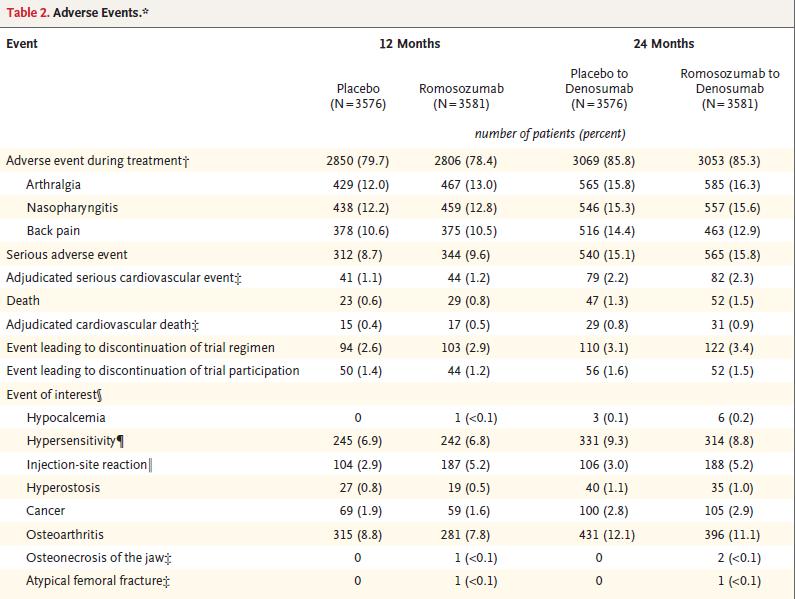
La incidencia de eventos adversos y eventos adversos graves fue similar en los dos grupos, al igual que la incidencia de eventos categorizados como osteoartritis, hiperostosis, cáncer, hipersensibilidad, y los eventos adjudicados como cardiovasculares graves (Tabla 2). Los eventos adversos graves que eran potencialmente indicativos de hipersensibilidad ocurrieron en 7 pacientes en el grupo de Romo durante el primer año. Se reportaron reacciones en sitio de inyección, en su mayoría leves, durante el primer año en 187 pacientes (5.2%) del grupo Romo y en 104 (2.9%) con placebo.
Se reportaron dos eventos compatibles con osteonecrosis de mandíbula en el grupo Romo. Un evento ocurrió después de 12 meses de tratamiento en un paciente con una prótesis desajustada, y el otro caso se produjo luego de una extracción dental con posterior osteomielitis, en un paciente que recibió de 12 meses de Romo y una dosis de Dmab. Se produjo una fractura atípica de fémur 3.5 meses después de la primera dosis de Romo (el paciente había informado dolor prodrómico en el sitio de inicio de fractura antes de la inclusión en el estudio).
Durante los primeros 15 meses del ensayo, 646 pacientes (18%) en el grupo de Romo desarrollaron anticuerpos anti-romosozumab, y 25 pacientes (0.7%) anticuerpos neutralizantes, sin detectarse efecto en la eficacia o seguridad de la droga. Los niveles medios de calcio sérico corregido por la albúmina fueron menores en el grupo Romo a 1 mes vs. el grupo placebo (cambio medio desde basal -2.2% vs. 0.0%).
DISCUSIÃN
En este estudio de fase 3 el tratamiento con Romosozumab en mujeres posmenopáusicas con osteoporosis, se asoció con un menor riesgo de nuevas fracturas vertebrales comparado con placebo a 12 meses. Este efecto fue rápido observándose solo 2 nuevas fracturas vertebrales en los segundos 6 meses del tratamiento (de un total de 16 de estas fracturas en el grupo con Romo en todo el período de 12 meses). También fue significativa la reducción del riesgo de fracturas clínicas (fracturas no vertebrales y fracturas vertebrales sintomáticas) en el grupo que recibió Romo por 12 meses vs. placebo. Debido al aumento de la morbilidad y costos en salud que generan las fracturas vertebrales y las fracturas clínicas, un tratamiento que permita reducir este riesgo rápidamente podrían ofrecer un importante beneficio a los pacientes.
Aunque todos los pacientes realizaron la transición a Dmab en el segundo año del ensayo, el riesgo de fracturas fue menor en el grupo que había recibido Romo en el primer año respecto al grupo que había recibido placebo, con menos fracturas vertebrales adicionales en el segundo año en los pacientes que originalmente recibieron Romo vs. el grupo que recibió placebo (5 vs. 25 fracturas), un patrón que también se observó para los demás tipos de fracturas. Estos resultados muestran que Romo se asoció con un riesgo de fractura subyacente más baja, incluso después de la transición a Dmab.
La tasa de fracturas no vertebrales en el grupo placebo fue menor que la esperada, lo que estuvo influenciado por una región geográfica con elevado número de pacientes incluidos (América Latina) en la que la incidencia de estas fracturas en el grupo placebo a los 12 meses fue un tercio de la tasa esperada, sin ningún efecto detectable del tratamiento, aunque este análisis de subgrupos por región requiere una interpretación cautelosa. Una observación es que la baja tasa de fracturas no vertebrales en el grupo placebo en la región de América Latina es consistente con valores bajos de FRAX basal en estas pacientes. En un análisis post hoc que incluyó a las pacientes fuera de América Latina, se observó una mayor tasa de fracturas no vertebrales en el grupo placebo y 12 meses de tratamiento con Romo se asoció a un riesgo de fractura 42% menor respecto a placebo. Estos resultados merecen una evaluación adicional.
Con respecto a los marcadores óseos los resultados confirman el doble efecto de Romosozumab al aumentar la formación y disminuir la resorción ósea por medio de la inhibición de la esclerostina. Este efecto de Romo en la formación y la resorción ósea se tradujo en grandes incrementos en la DMO en columna y cadera, y ya a los 6 meses, se observaron cambios clínicamente significativos. También se observó un incremento adicional luego de la transición a Dmab.
Los eventos adversos fueron similares en los dos grupos. Se observaron eventos adversos serios por reacciones de hipersensibilidad con Romo, aunque estos eventos fueron infrecuentes. Se reportaron casos de osteonecrosis de mandíbula y una fractura atípica de fémur, aunque fueron raros y ocurrieron en pacientes con factores de confusión que pueden haber contribuido con el evento o que plantean dudas acerca de la causalidad.
En conclusión, Romosozumab es un anticuerpo monoclonal que aumenta la formación de hueso y disminuye la resorción ósea. Un año de tratamiento con Romo en mujeres posmenopáusicas con osteoporosis, dio lugar a un menor riesgo de fracturas vertebrales y clínicas comparado con placebo. La mejora sustancial en la DMO en columna lumbar y cadera con Romo, proporcionan una base para una reducción continua en el riesgo de fractura con el tratamiento secuencial Romo-Dmab.
Figura 1. Régimen y evaluaciones del ensayo
Las mujeres fueron asignadas al azar, en una proporción de 1:1, para recibir Romo 210mg subcutáneo o placebo una vez al mes durante 12 meses (doble ciego). Luego, en período abierto, todas las pacientes recibieron Dmab 60 mg cada 6 meses subcutáneo por 12 meses adicionales, y la asignación inicial continuó siendo ciega. Las pacientes fueron estratificadas según la edad (<75 años y â¥75 años) y por la presencia o ausencia de fractura vertebral prevalente. En un sub-estudio que involucró a 128 pacientes, se evaluó la DMO al inicio y cada 6 meses y en un sub-estudio con 129 pacientes se evaluó los niveles de marcadores de recambio ósea al inicio del estudio, al día 14, ya los meses 1, 3, 3+14 días, 6, 6+14 días, 9, 12, 13, 18 y 24. Después del período de 24 meses, los pacientes continúan recibiendo Dmab en forma abierta en un estudio de extensión de 1 año (datos no mostrados).
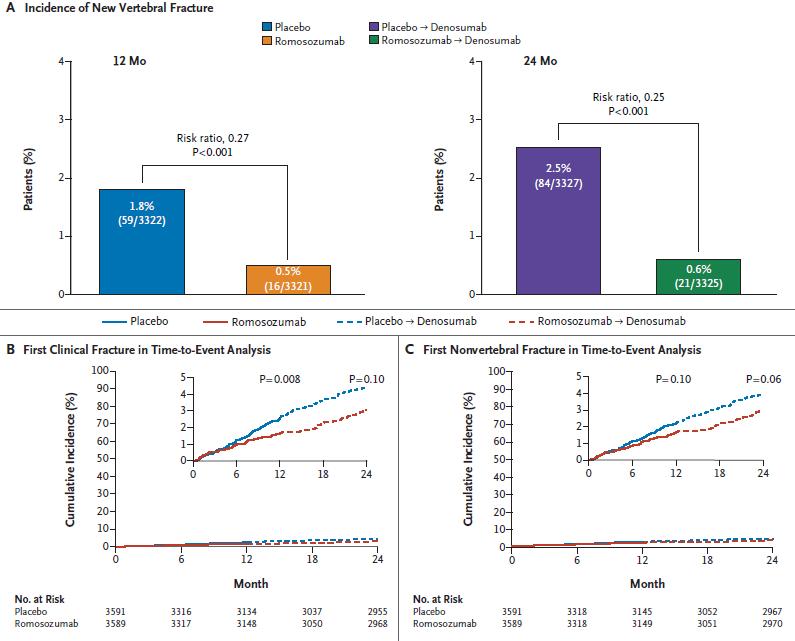
Figura 2. Incidencia de nuevas fracturas vertebrales, clínicas y no vertebrales.
Los end points primarios fueron la incidencia acumulada de nueva fractura vertebral a los 12 y 24 meses (Panel A). La evaluación del riesgo se realizó entre los grupos Romo vs. placebo a los 12 meses y a los 24 meses de Dmab. Se incluyen los datos de las pacientes randomizadas que tenían una radiografía basal y al menos una radiografía posterior. Curvas de Kaplan-Meier del análisis evento-tiempo de la primera fractura clínica (Panel B) y la primera fractura no vertebral (Panel C). Los recuadros muestran los mismos datos ampliados. Los valores de p son para los resultados a 12 y 24 meses y se basan en un modelo de regresión de Cox, con ajuste por edad y fractura vertebral prevalente, y ajustado para comparaciones múltiples.
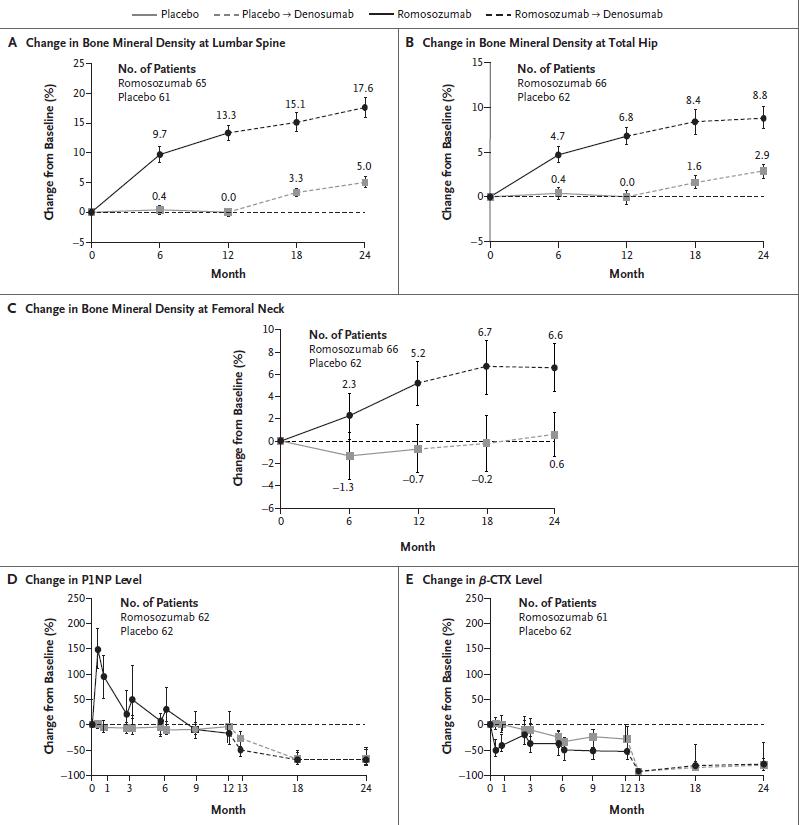
Figura 3. Porcentaje de cambio respecto al basal en la densidad mineral ósea y niveles de marcadores óseos.
Porcentaje de variación (media) para mínimos cuadrados de la DMO en la columna lumbar (Panel A), la cadera total (Panel B) y el cuello femoral (Panel C), para los 128 pacientes que participaron en el sub-estudio de DMO, que tuvieran una evaluación basal y al menos una posterior (dos pacientes [uno de cada grupo] no tenían la evaluación basal para la columna lumbar). Las comparaciones entre grupos, del porcentaje de variación medio desde basal en todos los tiempos de evaluación para todos los sitios esqueléticos mostraron p < 0.001. Se muestran las medianas del porcentaje de variación para los niveles de P1NP (Panel D) y β-CTX (Panel E) de las pacientes que participaron en el sub-estudio de marcadores óseos. Las barras I indican intervalos de confianza de 95% para los valores de DMO y rangos inter-cuartiles para los niveles de marcadores óseos, para los pacientes que tenían una medida basal y al menos una medición obtenida después. Las comparaciones entre grupos para porcentaje de variación de la DMO se analizaron con modelo de análisis de covarianza con ajuste para la DMO basal, equipo y la interacción de la DMO basal y el equipo. Comparaciones del porcentaje de variación medio desde basal para P1NP: p <0.001 a los 14 días ya los meses 1, 3, 3+14 días, 6+14 días y 13; y para mes 6 p = 0.33; mes 9: p = 0.95; mes 12 p = 0.006; mes 18 p = 0.74; y mes 24 p = 0.81. Comparaciones del porcentaje de variación medio con respecto al valor basal para β-CTX: p<0.001 a los 14 días ya los meses 1, 6+14 días, 9 y 12; y al mes 3 p = 0.25; mes 3+14 días p = 0.005; mes 6 p = 0.08; mes 13 p = 0.82; mes 18 p = 0.06; y el mes 24 p = 0.04. Para los niveles de P1NP y β-CTX, las comparaciones se calcularon con la prueba de suma de rangos de Wilcoxon.
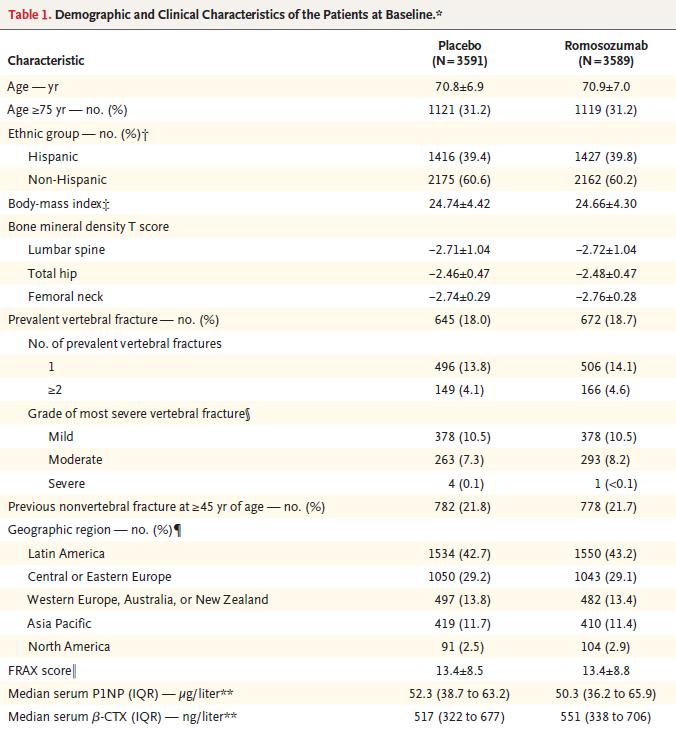
Tabla 1. Características basales demográficas y clínicas (media ± DS)*
*Los valores más/menos son medias ± SD. No hubo diferencias significativas entre grupos al inicio del estudio.β-CTX: isómero β de telopéptido del colágeno tipo I C-terminal, IQR: intervalo inter-cuartil y P1NP: propéptido del procolágeno tipo 1 N-terminal
â El grupo étnico fue auto-reportado.
â¡ El índice de masa corporal es el peso en kilogramos dividido por la talla en metros al cuadrado.
§ El grado de fractura vertebral más severa se evaluó con la escala de clasificación Genant.
¶ Los países incluidos en las respectivas regiones son los siguientes: América Latina: Colombia, Brasil, Argentina, República Dominicana y México; Europa central o del Este: Polonia, República Checa, Hungría, Lituania, Estonia, Letonia y Rumania; Europa oriental, Australia o Nueva Zelanda: Reino Unido, Dinamarca, Alemania, España, Nueva Zelanda, Suiza, Bélgica y Australia; Asia Pacífico: Japón, China (Hong Kong) e India; Y América del Norte: Estados Unidos y Canadá.
⥠El score según la Herramienta de Evaluación del Riesgo de Fractura (FRAX), desarrollado por la Organización Mundial de la Salud (www.shef.ac.uk/ frax/), indica el riesgo a 10 años de una fractura osteoporótica mayor.
** Los datos que se muestran corresponden a los pacientes incluidos en el sub-estudio de marcadores y biomarcadores óseos y que tuvieran mediciones de P1NP o β-CTX tanto basal como posteriormente y en una visita posterior (para el análisis de P1NP: 62 pacientes en cada grupo, y para el análisis de β-CTX: 62 pacientes en el grupo placebo y 61 en el grupo Romosozumab).
Tabla 2. Eventos adversos*
* Este análisis incluyo a totas las pacientes que fueron randomizadas y recibieron al menos una dosis de placebo o Romo en el período doble ciego de 12 meses iniciales.
â Los eventos enumerados son los eventos adversos más frecuentes que ocurrieron en el 10% o más de las pacientes en cualquiera de los grupos.
â¡ Incluyen los eventos adversos que fueron adjudicados como positivos por un comité de adjudicación independiente. Las muertes cardiovasculares incluyen eventos fatales que fueron adjudicados como cardiovasculares o indeterminados (presumiblemente relacionados con el corazón).
§ Eventos de interés fueron aquellos identificados por el Diccionario Médico Predefinido para las Actividades Regulatorias.
¶ Siete pacientes en el grupo de Romo presentaron eventos adversos graves durante el período doble ciego de 12 meses. Fueron reportados como relacionados con Romo: dermatitis, dermatitis alérgica y erupción macular. Todos resolvieron y la droga fue discontinuada en estos casos.
⥠Los eventos adversos más frecuentes en el sitio de inyección (en> 0.1% de los pacientes) en el grupo Romo fueron: dolor en el sitio de inyección (1.7%), eritema (1.5%), contusión (0.8%), prurito (0.7%), hinchazón (0.4%), hemorragia (0.4%), erupción cutánea (0.3%) y hematoma (0.2%).
Copyrigth2018 ENDOweb. Citar este artículo: Tratamiento con Romosozumab en mujeres posmenopáusicas con Osteoporosis – 17 de Nov 2016

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!