Teprotumumab para la oftalmopatía tiroidea
11 de septiembre 2017
Teprotumumab for Thyroid-Associated Ophthalmopathy. Smith TJ, et al. N Engl J Med 2017;376:1748-61.
INTRODUCCION
Son escasos los tratamientos para la oftalmopatía de Graves moderada a severa que hayan probado ser seguros y efectivos, y esto es en parte debido a la patogénesis de la enfermedad, incompletamente comprendida.
El receptor de la tirotrofina (TSH) es el blanco de auto-anticuerpos patógenos, conocidos como inmunoglobulinas estimulantes de la tiroides (TRAB), en la enfermedad de Graves. Estos auto-anticuerpos pueden detectarse en la mayoría de las personas que tienen esta enfermedad, con o sin oftalmopatía. La expresión del receptor de TSH en los tejidos orbitarios y por los fibrocitos de la órbita infiltrados, sugiere que contribuye a la oftalmopatía. Sin embargo, el hecho de que los TRAB no sean detectables en algunas personas con oftalmopatía sugiere que pueden estar implicados otros auto-antígenos.
En este sentido se han detectado inmunoglobulinas que activan el receptor del factor de crecimiento insulino símil tipo I (IGF-1) (IGF1-R). El IGF1-R es un receptor tirosinkinasa de membrana, que regula funciones del metabolismo y la inmunidad. Se encuentra sobre-expresado en los fibroblastos orbitarios y en linfocitos T y B de pacientes con enfermedad de Graves, formando un complejo de señalización con el receptor de tirotrofina a través del cual es trans-activado.
En estudios in vitro de fibroblastos orbitarios, se demostró que anticuerpos inhibitorios del IGF1-R podían atenuar las acciones del IGF1, tirotrofina y de los TRAB. Esto impulsó la realización de este estudio con teprotumumab, un anticuerpo monoclonal humano inhibidor del IGF1-R.
MÃTODOS
Se trata de un estudio prospectivo, randomizado, controlado con placebo y doble ciego. Incluyó pacientes entre 18 y 75 años, con oftalmopatía diagnosticada dentro de los 9 meses previos, con un Score de Actividad Clínica (CAS) ⥠4, en una escala de 0-7 puntos, (un CAS â¥3 indica oftalmopatía activa), sin tratamiento quirúrgico ni médico previo, con excepción de corticoides orales (una dosis acumulada ⤠1 mg de metilprednisolona o equivalente), y con un período de lavado de más de 6 meses.
Diseño. El estudio comprendió 3 fases:
Screening: 2 a 6 semanas
Intervención: 24 semanas
Seguimiento: 48 semanas
Objetivo primario: Evaluación de la proptosis y el score de actividad clínica (CAS) en semana 24.
Objetivo secundario: La evaluación sobre la calidad de vida usando un cuestionario de Calidad de Vida-Oftalmopatía de Graves (OG-QOL), con 2 sub-escalas: una que mide la calidad de vida afectada por las limitaciones en la función visual y la otra la afección psicosocial como consecuencia del cambio en la apariencia física.
El cuestionario tiene una escala de 1-100 puntos. Un cambio de 8 puntos se consideró relevante.
La diplopía subjetiva, fue evaluada con 4 grados, un cambio en 1 grado fue considerado relevante.
Se definió respuesta: como la disminución de 2mm o más en la proptosis, o reducción del CAS en ⥠2 puntos.
Alta respuesta se consideró cuando la proptosis se redujo 3mm o más y el CAS bajo más de 3 puntos.
Baja respuesta cuando la reducción fue entre 1 a 2mm en la proptosis, y el CAS bajó entre 1 a 2 puntos.
Sin respuesta cuando no hubo modificación o no se realizó la evaluación en la semana 24.
Se usó un modelo de regresión logística, con el grupo de intervención como modelo de efecto, y el hábito tabáquico como co-variable.
RESULTADOS
Se incluyeron 112 pacientes de los cuales se randomizaron 88 (24 no cumplían algún criterio de selección). 87 conformaron el grupo de “intención de tratar” que recibieron por lo menos una infusión:
45 pacientes recibieron placebo por 24 semanas (infusión endovenosa de solución salina). 39 (87%) completaron la intervención y el seguimiento.
42 pacientes recibieron teprotumumab por 24 semanas (8 infusiones endovenosas: 1 cada 3 semanas, con una infusión inicial de 10 mg/kg, y en las 7 restantes, 20 mg/kg). 37 (88%) completaron la intervención y 36 el seguimiento.
Los datos demográficos y características bioquímicas se detallan en la Tabla 1.
Tabla 1. Características de los pacientes basalmente
|
Características demográficas |
Teprotumumab N=43 |
Placebo N=44 |
|
Edad (años) |
51.6 ± 10.6 |
54.2 ± 13 |
|
Sexo Femenino (%) |
65% |
36% |
|
Tiempo de inicio tratamiento de enf. tiroidea en meses (mediana- rango) |
8 (1-134) |
15 (3-189) |
|
Tratamiento actual (%) |
||
|
Droga anti-tiroidea |
35% |
45% |
|
Levotiroxina |
60% |
52% |
|
Extracto tiroideo |
2% |
7% |
|
Duración de síntomas o signos oculares en meses |
4.7 ± 2.1 |
5.2 ± 2.3 |
|
Duración de la enfermedad de Graves en meses (mediana- rango) |
10.7 (1.2-228) |
10.8 (1.2-299) |
|
Estatus de tabaquismo (%) |
||
|
No fumadores |
74% |
59% |
|
Fumadores |
26% |
41% |
|
Características bioquímicas (%) |
||
|
Eutiroideos basalmente y en fase de intervención |
46% |
30% |
|
Valores ocasionalmente fuera de rango durante fase de intervención |
42% |
57% |
|
Valores sostenidamente fuera de rango durante fase de intervención |
12% |
14% |
Todos los pacientes estaban eutiroideos al inicio del estudio. Solo el 29%, requirieron un mínimo ajuste de la dosis de la levotiroxina o de la droga anti-tiroidea.
La proptosis, el CAS y el score de GO-QOL basal fueron casi idénticos en ambos grupos. Había mayor prevalencia de diplopía y tabaquismo en el grupo de teprotumumab.
En cuanto al objetivo primario, se observó “respuesta” en 29 de 42 pacientes (69%) del grupo que recibió teprotumumab, vs 9 de 45 pacientes (20%) en el grupo placebo, a las 24 semanas; p<0,001 (grupo intención de tratar).
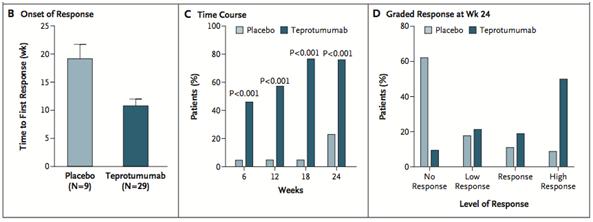
El tiempo para la primer respuesta fue marcadamente más corto en el grupo de teprotumumab vs placebo (Fig. 1B).
El comienzo de la respuesta fue rápido y la proporción de pacientes que tuvieron respuesta fue mayor en el grupo de teprotumumab vs placebo, en las semanas 6, 12 y 18 (p<0,001) (Fig. 1C). En el análisis del nivel de respuesta, hubo mayor proporción de “alta respuesta” en el grupo de teprotumumab vs placebo (p< 0,001 para las comparaciones en cada nivel de respuesta) (Fig. 1D).
Figura 1. Respuesta al tratamiento y seguimiento
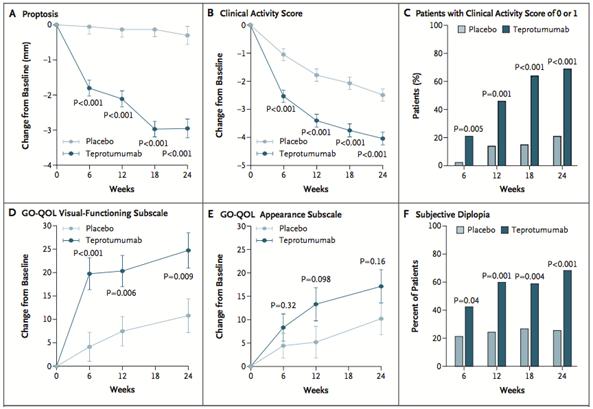
La reducción de la proptosis en la semana 6, 12, 18 y 24 fue significativamente mayor en el grupo tratado vs placebo (p<0,001) (Fig. 2A), de tal forma que un 40% (17 de 42 pacientes) habían reducido 4 mm o más su proptosis vs 0% del grupo placebo en la semana 24.
La reducción del CAS en semana 6, 12, 18 y 24 fue mayor en el grupo tratado vs el placebo p<0,001, aunque en el grupo placebo, también se vio una reducción progresiva, pero en menor grado. Un 69% de los pacientes con teprotumumab tenían un score de 0 o 1 en la semana 24 vs 21% del grupo placebo; p<0,001 (Fig. 2B y 2C).
El score GO-QOL, en la sub-escala de función visual, aumentó significativamente en el grupo de teprotumumab, unos 12.8 a 15.6 puntos más que el grupo placebo. En la sub-escala de apariencia hubo una tendencia a mejorar, pero no llegó a ser significativa (Fig. 2D y 2E).
Las tasas de respuesta de la diplopía subjetiva, también fueron significativamente mayores en el grupo tratado vs placebo p< 0,001 (Fig. 2F).
La eficacia también se evaluó en la semana 28 (7 semanas posterior a la última aplicación), y no hubo disminución de respuesta ni efecto rebote.
Figura 2. Puntos finales de eficacia secundaria
SEGURIDAD
Los efectos adversos se vieron en más de un 5% en el grupo de teprotumumab, y fueron más frecuentes en este grupo, respecto al grupo placebo. La mayoría fueron leves. La hiperglucemia fue el único evento adverso claramente identificado y relacionado con teprotumumab. En pacientes no diabéticos, la hiperglucemia fue intermitente, leve y similar en ambos grupos. En cambio, en pacientes diabéticos se observó hiperglucemia grado 2 a 3, que mejoró con el ajuste de la medicación antidiabética.
No hubo muertes durante el estudio. Los eventos adversos graves se produjeron en 5 de 43 pacientes (12%) en el grupo de la droga vs. 2% en el grupo placebo. Dos de ellos (diarrea y confusión mental), fueron catalogados como “posiblemente relacionados” con teprotumumab. Los otros eventos graves fueron catalogados como “no relacionados”.
DISCUSIÃN
Los pacientes que recibieron teprotumumab redujeron su proptosis y el CAS, y mejoraron el GO-QOL y la diplopía subjetiva en forma significativa en comparación con el grupo placebo.
La reducción de la proptosis fue similar a la reportada con la cirugía des-compresiva. Esto sugiere que la inhibición del IGF1-R, resulta en una disminución de la inflamación y el volumen de la grasa orbitaria, músculos o ambos. Aunque los autores reconocen que al no haber realizado estudios por imágenes, queda incierto qué tejido orbitario se vio afectado con el tratamiento.
En estudios in vitro, se observó un aumento de los anticuerpos activantes del receptor de IGF1 y sobre-expresión del receptor, en pacientes con enfermedad de Graves, pero otros estudios no lo demostraron.
Dada la evidencia, de que las acciones de la tirotrofina y los TRAB, son en parte dependientes de la actividad del receptor de IGF1, los beneficios clínicos reportados en este estudio podrían ser por la atenuación de la señalización patogénica mediada por ambos receptores: IGF1-R y TSH-R.
Es alentador el perfil de seguridad de esta droga, y coincide con lo reportado en estudios previos oncológicos. No hubo evidencia de empeoramiento residual del control glucémico después de la suspensión del tratamiento. Es posible que los pacientes diabéticos que reciban teprotumumab necesiten un mayor monitoreo glucémico y potencial ajuste de la medicación antidiabética.
Esta droga podría asociarse con diarrea y espasmos musculares en pacientes que tengan enfermedad gastrointestinal previa.
El trabajo tuvo limitaciones: sólo se incluyeron pacientes con enfermedad activa de reciente comienzo, con un CAS > de 4. Por lo que no fue evaluada la respuesta en pacientes con oftalmopatía leve o menos activa. Aun falta la fase de seguimiento del estudio (por un año), para poder evaluar la durabilidad de la respuesta.
En conclusión, un tratamiento de 24 semanas con teprotumumab benefició clínicamente a pacientes con oftalmopatía activa moderada a severa, reduciendo la proptosis y el score de actividad clínica y mejorando la calidad de vida del paciente.
Traducción y resumen: Dra. Lorena Conejos, médica especialista en endocrinología.

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!