La FDA aprueba un monitor de glucosa continuo implantable de 180 días
14 de febrero 2022
La FDA aprobó el monitor de glucosa continuo implantable (CGM) Eversense E3 de Senseonics, para su uso hasta por 6 meses.
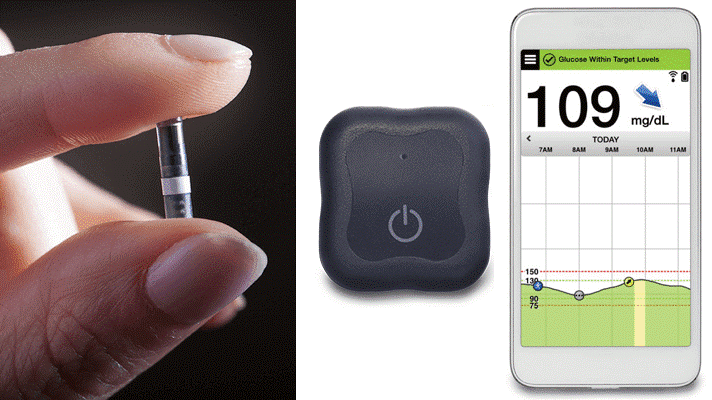
El sistema Eversense E3 está indicado para adultos mayores de 18 años con diabetes tipo 1 o tipo 2. Tiene el tamaño de un grano de arroz y una vez implantado por vía subcutánea en la parte superior del brazo bajo anestesia local, el sistema permite el reemplazo de las medidas de glucosa en sangre por punción en el dedo. La única vez que aún se requieren punciones en los dedos con este sistema es para la calibración, cuando los síntomas no coinciden con las lecturas de CGM o si el usuario está tomando un medicamento de la clase de tetraciclina.
Esta aprobación permite duplicar el tiempo de uso, ya que el sistema se aprobó inicialmente para un uso de 90 días en junio de 2018.
Al trabajar con el sensor implantado, el transmisor extraíble se mantiene en su lugar a través de un adhesivo a base de silicona y permite la transmisión de datos a una aplicación móvil donde los datos sobre valores de glucosa, tendencias y alertas se monitorean cada 5 minutos.
MARD (Mean Absolute Relative Difference) es el valor que mide en porcentaje la exactitud de un sensor y significa qué diferencia hay entre las mediciones del sistema a medir con respecto a otro sistema de referencia. Los MARD más bajos indican sensores más precisos. En general, cualquier valor inferior al 10 % se considera muy bueno. En el estudio PROMISE, que se presentó en las sesiones científicas virtuales de la American Diabetes Association (ADA) de 2021, el sistema CGM Eversense E3 demostró MARD del 8,5 % entre los valores de referencia clínicos y el sensor primario del dispositivo en base a casi 50 000 datos. El sensor fue más preciso al medir los rangos euglucémicos, con el MARD más alto informado con rangos hipoglucémicos (pudo alertar a los usuarios sobre casos de hipoglucemia con un 93 % de precisión). Pero todas las MARD se mantuvieron por debajo del 10 % para todos los rangos de glucosa en sangre.
Durante este estudio, el 90 % de los sensores duraron los 180 días completos de uso; el 96 % de los sensores alcanzaron una vida útil entre 90 y 120 días, y el 94 % hasta el día 150.
La implantación y extracción de los sensores se realizó sin problemas, sin eventos adversos graves relacionados con los dispositivos y solo el 1,1 % de los participantes del estudio experimentaron una infección leve en el sitio del implante después de que se extrajo.
Este cambio bioquímico que se ha realizado en el sensor es probablemente el camino a seguir en el futuro, ya que los pacientes podrán tener 6 meses de datos disponibles con un implante.
Senseonics dijo que se espera que el sistema CGM Eversense E3 esté disponible para los pacientes de EEUU a partir del segundo trimestre de este año.
Copyright 2022. Endoweb.net

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!