La FDA aprueba la primera hormona de crecimiento para administrar una vez por semana para niños
9 de septiembre 2021
La Administración de Drogas y Alimentos de los Estados Unidos (FDA) aprobó la lonapegsomatropina-tcgd (Skytrofa ®, Ascendis Pharma), la primera hormona del crecimiento inyectable subcutánea semanal para niños con deficiencia de la hormona del crecimiento (GHD) (1).
La aprobación se basó en los hallazgos del estudio heiGHt de fase 3; de 52 semanas de duración, en 161 pacientes pediátricos sin tratamiento previo con GHD, que se publicó recientemente en el Journal of Clinical Endocrinology & Metabolism (2).
Desde 1987, el tratamiento estándar para la GHD pediátrica ha sido una inyección diaria de somatropina (hormona del crecimiento humana de ADN recombinante).
Lonapegsomatropina está aprobada para el tratamiento de pacientes pediátricos de 1 año en adelante, que pesen al menos 11,5 kg y tengan baja estatura debido a la secreción inadecuada de la hormona del crecimiento endógena.
La molécula del fármaco consiste en un profármaco de somatropina que está inactivo ya que se une al portador inerte TransCon (conjugación transitoria). La molécula se rompe después de la inyección, exponiendo la somatropina activa, la cual se libera lentamente.
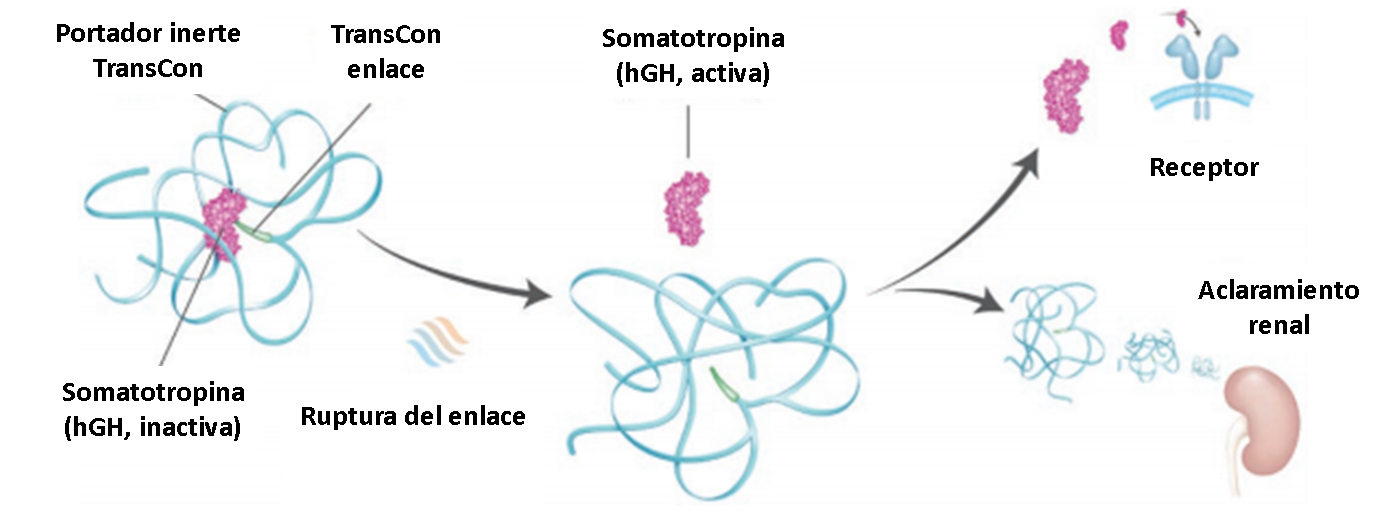
Fig 1: La lonapegsomatropina es un profármaco de acción prolongada que consta del fármaco original, somatropina no modificada; un portador inerte; y un enlazador que une temporalmente la somatropina y el portador. El portador tiene un efecto protector que minimiza la excreción renal y el aclaramiento mediado por receptores. Después de la autoescisión del enlazador en condiciones fisiológicas, la lonapegsomatropina libera de manera predecible somatropina dentro de los niveles terapéuticos durante una semana.
El ensayo heiGHt asignó al azar a niños prepúberes sin tratamiento previo con GHD 2: 1 a lonapegsomatropina semanal o somatropina diaria (Genotropin, Pfizer) en 73 centros de 15 países. Los niños tenían una edad media de 8,5 años (rango, 3,2-13,1 años), el 82% eran varones y el 94% eran blancos.
Este estudio demostró que la lonapegsomatropina no es inferior a las inyecciones diarias de somatropina. Los niños que recibieron lonapegsomatropina semanalmente crecieron 11,2 cm por año, mientras que los que recibieron una dosis total equivalente de inyecciones diarias de somatropina crecieron 10,3 cm por año.
Los resultados de seguridad (la relación entre la edad ósea y la edad cronológica, los eventos adversos, la tolerabilidad y la inmunogenicidad) fueron similares en ambos grupos. Ambos grupos de estudio informaron bajas incidencias de anticuerpos de unión anti-hGH transitorios no neutralizantes y ningún caso de anticuerpos persistentes.
No se informaron eventos adversos graves o interrupciones relacionadas con lonapegsomatropina. Las reacciones adversas más frecuentes en ⥠5% de estos pacientes pediátricos fueron infección viral (15%), pirexia (15%), tos (11%), náuseas y vómitos (11%), hemorragia (7%), diarrea (6 %), dolor abdominal (6%) y artralgias y artritis (6%).
Las limitaciones del ensayo incluyen el hecho de que el estudio no fue cegado (ya que los pacientes recibieron una inyección semanal o diaria) y las dosis del fármaco se fijaron en 0,24 mg de hormona del crecimiento humana / kg / semana, aunque en la práctica clínica real, las dosis pueden ajustarse.
La lonapegsomatropina se ha estudiado en más de 300 niños con DHC en el programa de fase 3 en el ensayo heiGHt (pacientes sin tratamiento previo), ensayo fliGHt (pacientes con experiencia en el tratamiento) y ensayo enliGHten (un ensayo de extensión a largo plazo en curso que incluye algunos pacientes que han estado recibiendo lonapegsomatropina durante más de 4 años).
Lonapegsomatropin-tcgd está contraindicado en múltiples poblaciones de pacientes, incluidos aquellos con enfermedad crítica aguda después de cirugía a corazón abierto, cirugía abdominal o trauma accidental múltiple, o insuficiencia respiratoria aguda debido al riesgo de aumento de la mortalidad con el uso de dosis farmacológicas de somatropina, aquellos con hipersensibilidad. a somatropina o cualquiera de los excipientes, y aquellos con cualquier malignidad activa.
Se espera que la lonapegsomatropina esté disponible en breve en los Estados Unidos y el resto del mundo, junto con un conjunto de programas de apoyo al paciente. El impacto de la aprobación de lonapegsomatropina en la práctica clínica dependerá de su disponibilidad, la cobertura de los proveedores de seguros de salud y la comodidad del paciente con el uso de un nuevo producto.
Para la mayoría de los endocrinólogos pediátricos, la hormona del crecimiento diaria ha estado disponible durante toda su carrera, por lo que espera que la comunidad de endocrinología pediátrica tarde algún tiempo en sentirse cómoda al recetar hormona del crecimiento de acción prolongada (LAGH), el nombre que se le da a los productos que se administran una vez a la semana. .Mientras tanto, se espera muy pronto una decisión de la FDA sobre otra hormona del crecimiento una vez por semana, el somatrogon (OPKO ® Health / Pfizer) para niños con GHD, en octubre de 2021. Por otro lado, un somapacitan inyectable semanal (Sogroya ®, Novo Nordisk), aprobado por la FDA en septiembre del año pasado para adultos con GHD, también se está estudiando en niños, y se estima que el estudio se completará en 2024.
Bibliografía:
1)https://www.fda.gov/drugs/new-drugs-fda-cders-new-molecular-entities-and-new-therapeutic-biological-products/novel-drug-approvals-2021
2) Thornton P y col. J Clin Endocrinol Metab. Publicado online el 17 de julio de 2021.

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!