La FDA aprueba el primer medicamento contra la enfermedad ocular tiroidea
19 de diciembre 2019
Esta semana se reunió el Comité Asesor de Drogas Dermatológicas y Oftálmicas de la FDA y aprobó teprotumumab para el tratamiento de la enfermedad ocular tiroidea (TED).1
La cirugía es hasta ahora el único tratamiento para la enfermedad activa, por lo que las infusiones de teprotumumab serían la primera opción de tratamiento farmacológico para una afección potencialmente cegadora y desfigurante.
Teprotumumab, un inhibidor del receptor del factor de crecimiento 1 similar a la insulina (IGF1-R), es un anticuerpo monoclonal completamente humano desarrollado para el tratamiento de TED, una enfermedad autoinmune progresiva que amenaza la visión. El teprotumumab bloquea la fisiopatología inflamatoria / autoinmune que subyace a TED, reduciendo la respuesta autoinmune e inflamatoria que conduce a la proptosis asociada con la orbitopatía de Graves.
El teprotumumab fue efectivo en dos estudios clínicos controlados 2, proporcionando mejoras estadísticamente y clínicamente significativas en múltiples facetas de esta patología. Una gran mayoría de pacientes logró mejoras sustanciales en proptosis, puntaje de actividad clínica (CAS), diplopía y calidad de vida con 24 semanas de terapia.
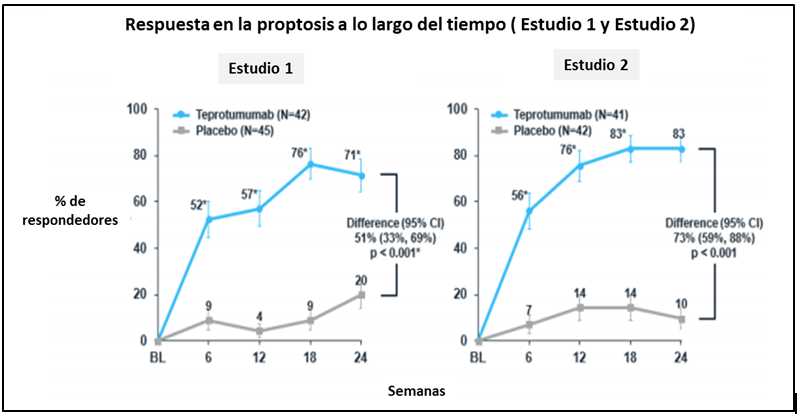
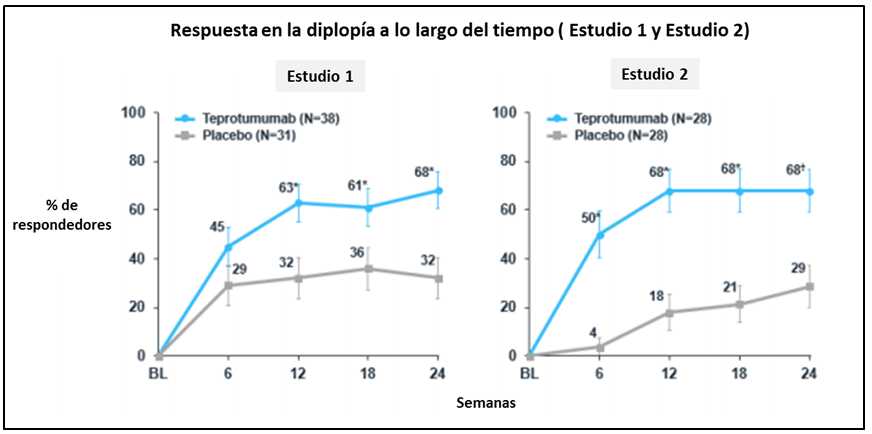
Sin embargo, 25% de los pacientes tratados con teprotumumab en los estudios clínicos experimentaron espasmos musculares, el evento adverso emergente del tratamiento más comúnmente reportado, aunque se desconoce cómo el medicamento podría causarlo. Los documentos informativos de la FDA sugirieron que este evento deberá estar incluido en Advertencia / Precaución de su prospecto.
Otros eventos notificados con frecuencia incluyen náuseas, alopecia, diarrea, fatiga, dispepsia, dolor de cabeza y piel seca. Alrededor del 7% de los pacientes también experimentaron hiperglucemia asociada con el tratamiento, que será un tema de discusión durante la reunión, en particular sobre si es necesario controlar la glucosa después de la infusión.
El comité discutió sobre otros eventos adversos emergentes del tratamiento, incluida la exacerbación de la enfermedad inflamatoria intestinal preexistente observada en dos pacientes tratados con teprotumumab en los ensayos del medicamento. La mayoría de los eventos adversos se clasificaron como leves o moderados y se manejaron en el contexto de los ensayos sin interrupción del tratamiento. Tomados en conjunto, los datos respaldan un perfil favorable de riesgo-beneficio para teprotumumab.
Bibliografía:
1) https://www.fda.gov/media/133431/download
2) American Association of Clinical Endocrinologists. Douglas R, et al "Teprotumumab treatment effect on proptosis in patients with active thyroid eye disease: Results from a phase 3, randomized, double-masked, placebo-controlled, parallel-group, multicenter Study" AACE 2019.
Copyright 2019. Endoweb.net

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!