La FDA aprueba el glucagón nasal para tratar la hipoglucemia grave
6 de agosto 2019
Esta semana la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó el glucagón nasal del laboratorio Eli Lilly1, que se venderá bajo el nombre de Baqsimi ®, la primera terapia de este tipo aprobada para el tratamiento de emergencia de la hipoglucemia grave, que se puede administrar sin necesidad de una inyección.
El objetivo de la formulación es reducir los minutos cruciales y el estrés del método actual para administrar esta hormona a personas con diabetes que sufren hipoglucemia grave, lo que puede provocar hospitalización o incluso la muerte en casos extremos. Baqsimi ® está aprobado para tratar la hipoglucemia grave en pacientes con diabetes de 4 años en adelante.
La formulación de glucagón que se utiliza actualmente requiere mezclar la droga que se encuentra en forma de polvo, e inyectarlo cuando una persona está experimentando una hipoglucemia grave, lo cual puede ser difícil, y con frecuencia el paciente necesita ayuda de un tercero.
Hay muchos productos en el mercado para aquellos que necesitan insulina, pero hasta ahora, las personas que sufrían un episodio de hipoglucemia severa tenían que ser tratadas con una inyección de glucagón que primero tenía que mezclarse en un proceso de varios pasos. Esta nueva forma de administrar glucagón puede simplificar el proceso, que puede ser crítico durante un episodio, especialmente porque el paciente puede haber perdido el conocimiento o puede tener una convulsión
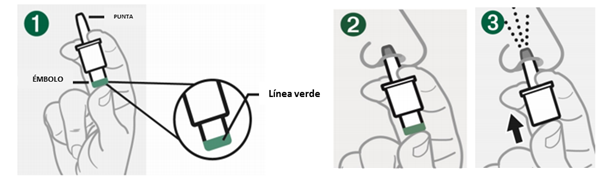
Baqsimi ® vendrá en un dispensador de un solo uso.
La eficacia y seguridad de Baqsimi para tratar la hipoglucemia grave se evaluó en 2 estudios de 83 y 70 adultos con diabetes, que compararon una dosis única de Baqsimi ® con una dosis única de la inyección de glucagón2. La nueva formulación nasal aumentó adecuadamente los niveles de glucosa. Se observaron resultados similares en un estudio pediátrico de 48 pacientes mayores de 4 años con DM13.
Luego de la administración de Baqsimi ® la glucemia aumentó hasta un valor medio de 140 mg/dl.
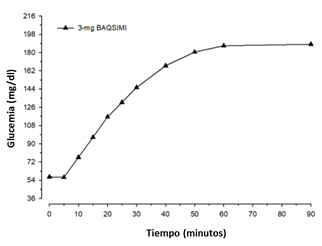
Concentración media de glucosa a lo largo del tiempo, luego de una dosis de glucagón nasal en un paciente con DM1 con una hipoglucemia inducida por insulina.
Baqsimi ® no debe usarse en pacientes con feocromocitoma, ni en pacientes con insulinomas. Debe ser usado con precaución por aquellos que han estado en ayunas durante largos períodos de tiempo, que tienen insuficiencia suprarrenal o hipoglucemia crónica debido a que estas afecciones se acompañan de baja producción hepática de glucosa.
Las reacciones adversas más comunes asociadas con Baqsimi ® son náuseas, vómitos, cefaleas, irritación del tracto respiratorio superior, congestión ocular y prurito.
Bibliografía:
1. https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=21013
2. https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=210134
3. Glucagon Nasal Powder: A Promising Alternative to Intramuscular Glucagon in Youth With Type 1 Diabetes. Sherr J. et al. Diabetes Care. 2016 Apr;39(4):555-62.
Copyrigth2019 ENDOweb. Citar este artículo: La FDA aprueba el glucagón nasal para tratar la hipoglucemia grave– 26 de julio 2019

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!