Inhibidores del transportador sodio-glucosa 2
15 de mayo 2017
Revisión de un tema
Por el Dr. Santiago Bruzone
INTRODUCCIÃN
Los inhibidores del transportador sodio-glucosa 2 (SGLT2i) son un grupo nuevo de fármacos desarrollados para el tratamiento de la diabetes tipo 2 (DM2). Ãstos nuevos antidiabéticos orales, además de disminuir la hiperglucemia mediante un novedoso mecanismo de acción, poseen efectos pleiotrópicos renales y cardiovasculares entre otros. A continuación veremos cuál es el mecanismo de acción de éstos fármacos, las características de los 3 SGLT2i disponibles, los efectos pleiotrópicos, el estudio EMPA-REG, y el rol que ocupan actualmente en el algoritmo de tratamiento de la DM2.
Filtración y reabsorción de glucosa
En el humano adulto un riñón normal filtra ~ 160-180gr de glucosa por día (tasa de filtrado glomerular: GFR), y casi toda o toda la glucosa se reabsorbe, siendo la excretada por orina menor al 1% (menos de medio gramo). Bajo condiciones normales, cuando la carga de glucosa excede los ~ 260-350 mg/min (“umbral de glucosa”, Tm), ésta comienza a aparecer en orina. Esta carga de glucosa en humanos no es un valor establecido, sino más bien un rango. Clásicamente los valores de concentración de glucosa plasmática requeridos para exceder el umbral de glucosa tubular es aproximadamente 180 mg% (pero el rango es muy variable oscilando desde 130 a 300 mg%). Este umbral aumentaría con la edad.
Existe un valor umbral de glucosa a la cual aparece en orina una vez que se alcanza el transporte máximo (Tm): concentración de glucosa a la cual el sistema de una nefrona se satura. Esto se debe a que algunas nefronas llegan al Tm antes que otras. El transporte renal máximo se alcanza en el punto al que todas las nefronas exceden su capacidad máxima de reabsorción de glucosa. En diabéticos, cuando el Tm se excede, habrá glucosuria.
El Tm está incrementado en diabéticos un 20-40% comparado con los no diabéticos, es decir el riñón capta más glucosa. Lo que fuera una respuesta adaptativa para asegurar suficiente ingesta calórica ahora es lo contrario: una mala adaptación que aumenta la glucemia.
El primer paso en la reabsorción de glucosa desde la orina es el pasaje desde la luz tubular a las células epiteliales tubulares, a cargo del SGLT. Se tratan de proteínas de membrana que transportan glucosa, aminoácidos, vitaminas, iones y osmolitos desde la membrana de reborde en cepillo del TCP y del intestino. Tanto la expresión como la función de los SGLT2 están aumentados en la DM 2.
Figura1. Reabsorción de glucosa del filtrado glomerular a través de la célula epitelial del TCP hacia la sangre. Clinical Diabetes 2010, Vol 28(1).
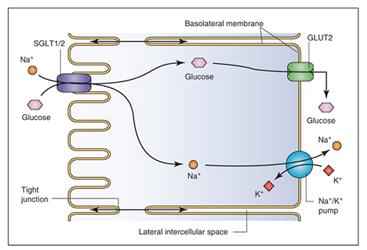
El segundo paso en la reabsorción de glucosa es su transporte desde la membrana basolateral desde la luz tubular al capilar peritubular. Esto se realiza a través de transportadores GLUT:
- GLUT1, en TCP distal
- GLUT2, en TCP proximal
Transportadores SGLT. Se distinguen:
- SGLT1: transportador de BAJA CAPACIDAD, ALTA AFINIDAD. En tracto gastrointestinal (GI) y TCP S3. Importante en tracto GI, en riñón solo es responsable del ~10% de la reabsorción de glucosa. Bajaría la absorción intestinal de glucosa y la glucemia postprandial.
- SGLT2: transportador de ALTA CAPACIDAD, BAJA AFINIDAD. En alta densidad en TCP S1. Responsable del ~ 80-90% de la reabsorción de glucosa. Se une al Na+ y glucosa y los trasloca a través de la membrana de las células apicales (transporte activo secundario, a través de un gradiente electroquímico de Na+ entre el filtrado tubular y la célula).
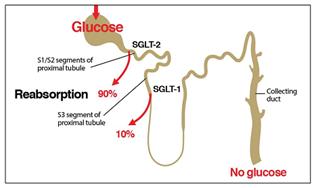
Figura 2. Manejo de la glucosa renal. Clinical Diabetes 2014, Vol 32(1)
Figura 2. En individuos sanos, la gran mayoría de la glucosa filtrada por el riñón es reabsorbida por SGLT-2 en los segmentos S1 y S2 del TCP, y la glucosa restante es reabsorbida por SGLT-1 en el segmento S3.
Como se sabe, los SGLT2 reabsorben un 80-90% de la glucosa filtrada y los SGLT1 el 10% restante. Pero los SGLT2i inducen una glucosuria máxima de hasta 50-80 g/d, unas 200-300 cal/día (sólo el 30-50% de la carga de glucosa filtrada en voluntarios sanos). No se explica porqué estos inhibidores no bloquean el 90% de la glucosa filtrada, causando una glucosuria mayor. Se propusieron varias teorías al respecto, pero la reciente explicación parece ser la más aceptada (Diabetología 2017 Feb;60(2):215-225):
- En normo-glucemia SGLT2 reabsorbe ~97% de la glucosa filtrada y SGLT1 reabsorbe un ~3%. Es decir que de un 0-0.2% de la glucosa se excreta por orina. Al inhibir SGLT2, la reabsorción de la glucosa es más distal, desenmascarando una significativa capacidad de SGLT1 para reabsorber ~50% de la glucosa filtrada.
- En hiperglucemia aumenta tanto la cantidad de glucosa filtrada por los riñones como la capacidad de reabsorción renal tubular en un 20% (500-600 g/día en diabéticos tipo 1 y 2). Si el filtrado glomerular (FG) es normal y la glucemia se encuentra entre 180-216 mg%, los riñones reabsorben toda la glucosa filtrada; solo en aumentos mayores se observa un aumento lineal en la glucosuria. Este aumento en la reabsorción renal de glucosa tiene sentido para conservar el ahorro de energía, pero es contraproducente en la diabetes ya que contribuye a la hiperglucemia. Entonces la diabetes induce hipertrofia tubular, la cual se asocia a aumento (up-regulation) de SGLT2. En consecuencia, esto puede contribuir a hiperglucemia y a hiperreabsorción tubular primaria de Na+. La inhibición de SGLT2 contrarresta estos efectos y favorece una compensación parcial por los SGLT1 distales.
INHIBICION DE SGLT2
La inhibición de la reabsorción tubular renal de glucosa (a través de los inhibidores de la reabsorción), lleva a un descenso de la glucemia a través del aumento de su excreción renal, que con los inhibidores llega al darse a los ~ 70-90 mg%. Esto se trata de una novedosa terapia antidiabética eficaz independiente del grado de insulino-resistencia, presencia de insulina, y magnitud de la falla celular beta. Esta inhibición demostró ser igualmente eficaz tanto en diabéticos de reciente diagnóstico, como en diabéticos con más de 10 años de enfermedad. Además demostró beneficios adicionales tales como: pérdida de peso, baja índice de hipoglucemia, y reducción de la presión arterial (PA).
Los SGLT2i disponibles a la fecha en Argentina son tres: dapagliflozin, canagliflozin, y empagliflozin. A continuación se resumen los efectos que producen éstos fármacos sobre parámetros metabólicos y sobre la función renal y cardiovascular: (Clinical Diabetes 2014, Vol 32(1). Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy 2013:6)
- Reducción de A1c: 0.8-1% solos o en combinación (o puede más de 1% cuanto más alta es la A1c, esto se vio con 3 estudios con dapagliflozin).
- Función renal: la tasa de FG es un factor determinante para que los inhibidores del SGLT produzcan glucosuria. A medida que baja el FG, la eficacia de inhibidor disminuye.
- Reducción de peso: en estudios de hasta 104 semanas, de fase 2 y 3, se han observado reducciones de hasta 5 kg. En pacientes en estadios más avanzados de su DM2 (con insulina a altas dosis más antidiabéticos orales) el descenso fue de 4.3 a 5.05 kg; mientras que en estadios más tempranos fue de 2 a 2.5 kg. Se vio que atenúan la ganancia de peso asociada con pioglitazona o insulina. La pérdida de peso se acompaña por una pérdida de grasa corporal (visceral y subcutánea), aproximadamente â de masa grasa en vez de masa magra, y más visceral que subcutánea (esto fue observado por absorciometría dual de rayos X, DXA). El descenso de peso se vio principalmente en las primeras semanas de tratamiento con dapagliflozin (la pérdida de peso estaría dada por pérdida de fluido, más pérdida de masa grasa).
- Reducción de PA: se observaron descensos ~ 2-10 mmHg en la PA sistólica. En PA diastólica los descensos fueron menores (0.88 a 3.5 mmHg). Estos efectos no fueron dosis dependientes y no se acompañaron de cambios en la frecuencia cardíaca o en incremento de la hipotensión arterial ni síncope.
- La reducción inicial de la PA se cree es por la diuresis osmótica por la inhibición de la reabsorción de glucosa y Na+. Esto implica un mayor pasaje de Na+ por el TCD. Las células de la mácula densa sensan el aumento del Na+ e inhiben a las células yuxtaglomerulares para la liberación de renina. Esta inhibición del sistema RA puede reducir la PA y dar nefroprotección debido a la disminución de la PA intraglomerular e hiperfiltración. Si bien este mecanismo de excreción de Na+ está levemente disminuido por estos fármacos, debido a un mecanismo de feedback túbulo-glomerular, el balance en la excreción de Na+ aun da positivo con el uso crónico de estos fármacos. Esto debe ser estudiado en humanos.
- Reducción en niveles de ácido úrico: podría tratarse de un efecto beneficioso adicional debido a que la hiperuricemia es un factor de riesgo independiente para hipertensión arterial, insuficiencia renal, y enfermedad cardiovascular. Este efecto estaría mediado a través de los receptores GLUT9 en la membrana apical de TCP, los cuales intercambian glucosa por uratos. La alta concentración de glucosa en el túbulo favorecería el intercambio de glucosa por uratos.
- Los descensos fueron entre 5.9%-17.8% tanto en monoterapia como combinados. Pero cuando su uso fue combinado con insulina el descenso fue menor (3.86%-4.9%), probablemente debido a los efectos hiperuricémicos del hiperinsulinismo.
- Lípidos: canagliflozin mostró en varios estudios un â HDL (7.1%10.6%), â LDL (7.1%), y â TAG (2.3%).
- Densidad mineral ósea: se han observado algunos cambios en los marcadores de resorción y formación ósea.
SEGURIDAD Y TOLERABILIDAD. Clinical Diabetes 2014, Vol 32(1). Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy 2013:6.
Para dapa, cana y empagliflozin, la incidencia de eventos adversos (EA) (combinados o no) fue de 1% a 12.6 %, siendo canagliflozin el de mayor porcentaje. Solo hubo que discontinuar la droga en 0.9- 9.9% de los casos.
- Infecciones genitales: el hecho de favorecer la glucosuria crea una ambiente para el crecimiento de gérmenes en el tracto urinario (principalmente micóticas).
- Infecciones del tracto urinario (ITU): algunos estudios han mostrado aumento de la incidencia de ITU (3-13%), pero en muchos casos estas infecciones no fueron verificadas con cultivos; mientras que otros estudios la tasa fue igual a placebo. En general fueron más frecuentes es mujeres, y no parecen ser dosis dependientes (en algunos casos con 5 mg de canagliflozin fueron mayores que con 10 mg).
- Infecciones genitales: solos algunos estudios demostraron el doble de casos de vulvovaginitis y balanitis (principalmente en no circuncidados), y también fueron más frecuentes en mujeres, leves a moderadas (infecciones genitales: 7.4-25%, mujeres 2.5 a 8%). En la mayoría de los casos respondieron al tratamiento convencional, y la droga de estudio no fue discontinuada (menor a 1%). Tanto las ITU como las infecciones genitales ocurrieron dentro del año de tratamiento y tuvieron bajas tasas de recurrencia (menor a 1%).
- Depleción de volumen e hipotensión ortostática: incidencia menor al 3%, y fueron leves a moderadas. Se debe tener especial cuidado en pacientes ancianos, y pacientes medicados con diuréticos, inhibidores ARA II e inhibidores de la enzima convertidora de angiotensina (ECA).
- Hipoglucemia: incidencia del 0.9-4.3% en monoterapia, que aumentó al 6% combinado con metformina. Fue severa en menos del 1% de los casos.
- El efecto glucosúrico de los inhibidores está relacionado a la carga de glucosa. Una vez que la carga de glucosa es â¤80 g/día (carga que puede ser controlada por SGLT1), se tornan inefectivos.
- Recientes publicaciones (Diabetología 2017 Feb;60(2):215-225): informan nuevos datos sobre SGLT2 y sobre la capacidad residual de SGLT1: en humanos o animales euglucémicos los SGLT2 reabsorben un 97% de la glucosa filtrada al inhibir al SGLT2, ¿cómo es que todavía mantienen una capacidad de reabsorción de glucosa del 50%, y no mayor?. Se observó en ratones que la inhibición de SGLT2, al aumentar la carga de glucemia distal en TCP, desenmascara una significativa capacidad del SGLT1 para transportar glucosa, limitando la glucosuria y la hipoglucemia. Además, los SGLT2i aumentan la glucagonemia y la gluconeogénesis hepática en diabéticos tipo 2.
- También, los SGLT2i aumentan la lipólisis y cambian la utilización de sustratos de los carbohidratos a los lípidos (contribuyendo así a reducir la masa grasa y el peso). Todas estas respuestas contribuyen a prevenir la hipoglucemia.
- Laboratorio:
- Función renal: no se evidenció alteración pese a un aumento de la creatinina del 1-6%, y descenso de la tasa de filtración glomerular estimada (eGFR) del 1-5%, pero que luego se recupera
- Función hepática: solo con canagliflozin se vio descenso de GPT y γ GT del 3-15% para ambas
- Hematocrito: se vio un aumento del 1-2%, que sería por la leve contracción de volumen
CARACTERISTICAS DE LOS DISTINTOS SGLT2i
Dapagliflozin
Dosis: Se administra una vez al día una tableta de 10 mg. Dosis de 5 mg (no disponible en Argentina) si hay alteración en la función hepática. Se ingiere con medio vaso de agua, con o sin alimentos, en cualquier momento de día.
Ante un olvido en la toma: si faltan más de 12 horas para la siguiente toma, debe ingerirse, y en caso contrario omitir la dosis.
Edad: indicado entre los 18 y 75 años de edad.
- Se desaconseja si el clearance de creatinina es menor a 60ml/min y la eGFR es menor a 60 ml/min/1.73 m2
- Insuficiencia hepática grave: iniciar 5 mg, y si se tolera bien se puede subir a 10 mg diario
- No indicar si se usan diuréticos de asa o en ancianos
No se recomienda indicarlo con pioglitazona (por riesgo de cáncer de vejiga).
Canagliflozin
Dosis: 100 mg una tableta previa al inicio de la primer comida del día. Se puede aumentar al 300 mg una tableta por día (solo si el eGFR es â¥60mL/min/1.73 m2).
Insuficiencia renal:
- eGFR 45 a 60mL/min/1.73 m2: dosis máxima 100 mg/día.
- Si recibe inductores enzimáticos de la UDP-glucuronosyl transferasa (rifampicina, fenitoína, fenobarbital, ritonavir) y el eGFR es entre 45 y 60, considerar otra terapia.
- eGFR < 45 mL/min/1.73 m2. No se recomienda iniciarlo.
- eGFR < 30 mL/min/1.73 m2, o diálisis: contraindicado.
Insuficiencia hepática: si es leve y moderada no requiere ajuste de dosis. Si es severa (Child-Pugh clase C): no se recomienda (no fue estudiado).
Empagliflozin:
- Dosis: dosis inicial 10 mg/día. Se puede incrementar a 25 mg/día (ver luego estudio EMPA-REG).
- Insuficiencia renal:
- eGFR ⥠30mL/min/1.73 m2, no requiere ajuste de dosis.
- eGFR menor a 30 (o diálisis): contraindicado.
- Insuficiencia hepática: puede indicarse.
En resumen, los SGLT2i se desaconsejan o contraindican en pacientes mayores a 75 años, con insuficiencia renal, diabéticos tipo1, y uso concomitante de diuréticos de asa. Son ideales para el tratamiento de diabéticos tipo 2, con sobrepeso u obesidad, combinado con otros antidiabéticos orales (o insulina), y como se verá luego, en pacientes con enfermedad cardiovascular y/o renal debido a sus recientemente descriptos efectos pleiotrópicos renales y cardiovasculares.
Inhibidores duales SGLT1 y 2. Diabetes & Vascular Disease Research 2015, Vol 12(2):101-110
El SGLT1 es el principal responsable de transportar la glucosa para su absorción en el tracto GI. Similar al SGLT2 en el riñón, el SGLT1 está sobre-expresado en el tracto GI de pacientes con diabetes tipo 2.
En ratas sin el SGLT1 se observó una marcada reducción de la hiperglucemia postprandial. La glucosa llega más distal en intestino, donde las células L detectan más glucosa, liberando GLP-1, y péptido YY.
Estudios preclínicos y clínicos demostraron que sotagliflozin es un inhibidor dual de SGLT1 y 2, reduciendo tanto la glucemia pre y post prandial. Actualmente se encuentre en fases avanzadas de investigación.
WARNINGS FOOD AND DRUG ADMINISTRATION (FDA)
Se debe alertar al paciente si presenta signos o síntomas de cetoacidosis diabética (CAD), de infecciones del tracto urinario, o factores de riesgo para fracturas.
1- CETOACIDOSIS DIABETICA. El 5/5/15, la FDA emitió una advertencia, informando que el tratamiento con inhibidores de SGLT2 (dapa, cana y empagliflozin) pueden aumentar el riesgo de CAD. La mayoría de los pacientes eran diabéticos tipo 2, y la glucemia estaba levemente elevada. En algunos reportes se informaron probables factores predisponentes: enfermedad subyacente, reducción de ingesta de líquidos y comida, y reducción en la dosis de insulina. Pero en la mitad de los casos no se encontró factor desencadenante. El tiempo medio de aparición de CAD fue de 14 días desde el inicio de la droga. Las glucemias en general no fueron mayores a 200 mg%. La Agencia Europea de Medicamentos (EMA), hasta mayo de 2015, reportó 101 casos de CAD en diabéticos tipo 2, con una exposición estimada de 0.5 millón de paciente-año. Todos los casos fueron serios, y algunos requirieron hospitalización. En algunos casos la elevación de la glucemia fue moderada. Diabetes Care 2015;38(9):1638-1642.
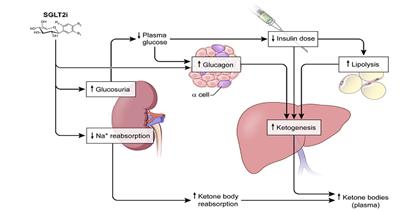
Fisiopatología probable de CAD. J Clin Endocrinol Metab, 2015; 100(8):2849-2852
Figura 1. Mecanismos potenciales donde la terapia adyuvante con SGLT2i puede promover cetosis e incrementar el riesgo de cetoacidosis en paciente con DM 1. Los SGLT2i disminuyen la glucosa por mecanismo independiente de la insulina. Para minimizar el riesgo de hipoglucemia, los pacientes DM1 pueden necesitar disminuir la dosis de insulina, la cual se supone que incrementa la tasa de lipólisis en el tejido adiposo y la cetogénesis hepática. Además SGLT2i demostraron incrementar los niveles de glucagon en plasma en DM 2, posiblemente para compensar la excresión de glucosa urinaria. Recientemente se ha reportado que los SGLT2i aumentan la la expresión del gen de preproglucagon actuando directamente en las células α del páncreas. Phlorizin (un inhibidor no selectivo del SGLT1 y SGLT2) demostró incrementar la reabsorción tubular renal de acetoacetato. Si los SGLT2i selectivos tienen esta acción, es posible que también puedan disminuir el clearance renal de cuerpos
Un reporte reciente (Bonner et al. Nat Med 2015; 21:512-27), informa que los SGLT2 (y SGLT1) se expresan en células α, y que este transportador funcionaría como un glucosensor de estas células. Informa además que la exposición de dapagliflozina a islotes humanos de células α aumentó la secreción de glucagón. Esto podría a su vez llevar a un aumento en la producción de cuerpos cetónicos.
La evidencia sugiere que el riesgo de CAD euglucémica, glucemia menor a 250 mg%, en pacientes DM2 que reciben SGLT2i sería muy bajo, con “aceptable” frecuencia. El riesgo podría aumentar en DM2 de larga data (con marcada disminución de la función de la célula β) o LADA, y durante períodos de baja ingesta, cirugías o enfermedades intercurrentes.
Rosenstock y Ferrannini, sugieren que la CAD relacionada a la inhibición del SGLT2 es predecible, detectable y prevenible (o mitiagable), y que los beneficios de uso de los SGLT2i en los diabéticos tipo 1 son mayores que los riesgos.
Inicialmente puede haber hipercetonemia inducida por distintas causas (reducción o aumento de la demanda en la dosis de insulina, estrés, etc.). El paciente puede no sentirse bien y tener náuseas sin vómito. Se controlará la glucemia, que estará levemente elevada por la persistente glucosuria. Evitará comer y reducirá o mantendrá la insulina, lo que aumentará los cuerpos cetónicos y elevará el riesgo de CAD. Habrá depleción de volumen por la glucosuria y vómitos.
Ante un paciente que no se sienta bien, sería entonces conveniente medir cetonemia y cetonuria. Si se detectaran y existen náuseas o vómitos (o malestar luego de ingesta de alcohol o reducción de dosis de insulina), se podría aumentar la dosis de insulina, suspender el inhibidor SGLT, y aumentar la ingesta de hidratos de carbono y líquidos, hasta que la cetosis resuelva. Diabetes Care 2015;38(9):1638-1642.
Se recomienda que los diabéticos tipo 1 firmen consentimiento informado para el uso de estos fármacos, ya que están contraindicados.
2- UROSEPSIS O PIELONEFRITIS. Desde marzo/2013 a enero/2014 se identificaron 19 casos, que se iniciaron como infección del tracto urinario (ITU) y debieron ser hospitalizados (unos pocos requirieron UTI o diálisis).
3- INSUFICIENCIA RENAL AGUDA (IRA) (FDA 6/16). Desde marzo/2013 hasta octubre/2015 la FDA recibió 101 casos confirmados de IRA (algunos que requirieron hospitalización y diálisis), con cana o dapagliflozin. Al respecto se recomienda:
- Evaluar función renal previo a indicar cana o dapagliflozin y considerar factores que puedan predisponer a IRA tales como: disminución del volumen sanguíneo, IRC, insuficiencia cardíaca congestiva y medicaciones concomitantes tales como diuréticos, IECA, ARAII, AINES
- Monitorear la función renal periódicamente
- Si ocurre IRA, suspender la droga e instaurar tratamiento
4- FRACTURAS ÃSEAS. Se observó aumento no significativo en su incidencia principalmente con canagliflozin. La ADA 2016 recomendó evitar su uso en pacientes con factores de riesgo para fracturas. No se observó con empagliflozin y dapagliflozin. Posibles mecanismos serían las caídas por hipotensión ortostática y la disminución de la densidad mineral ósea, en cadera y columna lumbar observada a lo largo del tiempo.
5- AMPUTACIONES. La FDA está estudiando el aumento de la incidencia de amputaciones (de miembro inferior y pies, especialmente dedos) observada en un estudio on-going con canagliflozin. Aun no se ha establecido una relación causal.
6- CÃNCER DE VEJIGA. El cáncer de vejiga ocurre más frecuentemente en pacientes tratados con dapagliflozin: 9 casos en 5478 pacientes (0.16%) vs. 1 caso en 3156 controles (0.03%). El número de casos fue muy pequeño para establecer causalidad. Se postula que los elevados niveles de glucosa en vejiga acelerarían la tasa de crecimiento de un cáncer preexistente.
- La mitad de los cánceres fueron encontrados dentro de los 6-12 meses de iniciado el tratamiento.
- 6 de 9 casos tenían hematuria demostrada desde el inicio del tratamiento (ya tenían alguna lesión?).
Por lo tanto se indica no utilizar éste fármaco en pacientes con antecedentes previo o con cáncer activo de vejiga.
EMPA-REG OUTCOME TRIAL. N Engl J Med 2015;373:2117-2128
- 7020 pacientes con DM2 con enfermedad cardiovascular (CV) establecida y su terapia standard, randomizados a recibir 10 o 25 mg de empagliflozin vs placebo (tiempo medio de observación: 3.1 años). El clearance de creatinina fue â¥30 ml/min. El 80% de los enrolados recibieron IECA o ARAII.
- El outcome primario compuesto fue: muerte cardiovascular, IAM no fatal, stroke no fatal. El secundario fue el primario más hospitalización por angina inestable.
- Resultados:
- El outcome primario ocurrió en 10.5% con empagliflozin vs 12.1% placebo (HR en el grupo empa: 0.86; 95.02% IC, 0.74 a 0.99; P = 0.04 para superioridad).
- El outcome secundario ocurrió en 12.8% con empa vs. 14.3% con placebo (HR en el grupo empa: 0.89; 95% IC, 0.78 a 1.01, p<0.001; para no inferioridad y p=0.008 para superioridad).
- No hubieron diferencias significativas en las tasas de IAM o stroke no fatales entre ambos grupos.
- Muerte de causa cardiovascular: diferencia significativa 3.7% vs 5.9%, 38% de reducción de RR.
- Hospitalización por insuficiencia cardíaca: diferencia significativa 2.7% vs 4.1%, 35% de reducción de RR.
- Muerte de cualquier causa: diferencia significativa 5.7% vs 8.3%, 32% de reducción de RR.
- Reducción de nefropatía o empeoramiento de ésta (definida como progresión a microalbuminuria, duplicar el valor de creatinina, inicio de diálisis, o muerte por enfermedad renal), 39% de reducción de RR.
- El los grupos de tratamiento se observaron más infecciones genitales, pero no de otros eventos adversos.
- Por lo tanto, en pacientes con diabetes tipo 2 y alto riesgo cardiovascular, la adición de empagliflozin a la terapia estándar retrasó la progresión de enfermedad renal y bajó los eventos cardiovasculares y renales clínicamente relevantes.
- Los Hazard ratios para outcomes CV para ambos grupos con empagliflozin fueron similares. Por lo tanto la dosis se elegirá según parámetros metabólicos y de EA.
- Se infiere que los efectos positivos CV serían multicausales: reducción de la albuminuria, reducción del ácido úrico, reducción de la glucemia, en el peso y en la grasa visceral, reducción en la presión arterial (PA), reducción de la rigidez arterial, cambios en la función cardíaca, demanda cardíaca de oxígeno (en ausencia de activación nerviosa simpática), y efectos cardiorrenales.
PROTECCIÃN RENAL Y CV DE LOS SGLT2. Diabetología 2017 Feb;60(2):215-225
Una posible explicación para los efectos protectores renales y CV de la inhibición de los SGLT2 es la asociación de efectos pleiotrópicos; la inducción de múltiples procesos que tienen beneficios sinérgicos, como por ejemplo los observados en el estudio EMPA-REG: mejoras en el control glucémico, reducciones en el peso, cintura abdominal, ácido úrico, PA sistólica (PAs) y diastólica, (PAd) (sin aumento de la frecuencia cardíaca).
Se destaca que los efectos beneficiosos CV ocurren al poco tiempo de iniciada la terapia, a diferencia de lo observado con otros fármacos. A continuación se describen los probables mecanismos por los cuales éstos fármacos confieren los efectos beneficiosos.
- Descenso de la hiperglucemia. Si bien este efecto es pequeño, reducen la glucotoxicidad renal y extra-renal. (Cardiovasc Diabetol 2016, 15:85). Pero como la reducción en la glucemia es pequeña, el impacto protector CV es débil. Además el rápido efecto protector de estos fármacos no se condice con el descenso de la glucemia.
- Reducción de la PA. Se observó en un meta-análisis en DM2 (consistente con lo observado en estudios pre-clínicos y en el EMPA-REG), un descenso de 3-6 mmHg en la PAs. Estos descensos son comparables con los observados con algunos agentes anti-HTA. Este efecto anti-HTA se debería a: 1) efecto natriurético, 2) descenso de peso, y 3) diuresis osmótica modesta (100-400 ml/día) basada en la glucosuria. Al reducir la PA y el volumen plasmático, rápidamente reducen la pre y post carga cardíaca, potencialmente contribuyendo a los rápidos beneficios cardíacos observado con estos fármacos. Particularmente en pacientes con insuficiencia cardíaca (IC) se observó un descenso de un 35% en hospitalización por IC (Cardiovasc Diabetol 2016, 15:85). Estos efectos serían compatibles con la temprana divergencia de las curvas de sobrevida CV. En contra de esta hipótesis está la tendencia observada hacia un aumento del riesgo de un stroke no fatal (esto es sorprendente ya que el stroke es la complicación macrovascular que más se beneficiaría del descenso de la PA).
- Pérdida de peso. De los 2-3 kg que se pierden, la pérdida de fluídos es el componente inicial, luego cobra importancia la pérdida de grasa. Se reportó un descenso en la grasa subcutánea y visceral en pacientes diabéticos tipo 2 tratados con SGLT2 (Cardiovasc Diabetol 2016, 15:85). Al igual que con el descenso de la glucemia, el descenso de peso no explica el rápido efecto protector sobre la mortalidad CV.
- Inhibición de la hiperuricemia. Se hipotetizó que la glucosa en el lumen del TCP puede facilitar el intercambio intracelular de uratos vía el transportador de uratos GLUT9 isoforma 2, aumentando la excreción urinaria de uratos.
- Otros mecanismos (Cardiovasc Diabetol 2016, 15:85).
- Aumento de consumo cardíaco de β-hidroxibutirato. Ante condiciones del aumento de liberación de glucagón, existe una leve y persistente hipercetonemia tal como fue reportado por Ferrannini y col. El β-hidroxibutirato puede ser tomado libremente y oxidado por el corazón en preferencia a los ácidos grasos. Esta selección de combustible puede mejorar la transducción del consumo de O2 en un trabajo eficiente a nivel mitocondrial. Además, la hemoconcentración que sigue a la inhibición de SGLT2 favorece la liberación de O2 a los tejidos, estableciendo una potente sinergia con el cambio del sustrato metabólico y que finalmente explique el efecto beneficioso CV observado en el EMPA-REG.
- Rigidez arterial. Se reportaron reducciones en la rigidez arterial en diabéticos tipo 1 normotensos.
- Efecto antiarrítmico. Posible efecto indirecto, mediado por glucagón.
- Efecto mediado por inhibición del SRAA. La mayoría de los sujetos del EMPA-REG fueron tratados con drogas activas sobre el SRRA. Estos fármacos combinados con los inhibidores del SGLT2 tendrían efectos positivos sobre la hemodinamia glomerular y nefroprotección, activando las vías del receptor AT2 y angiotensina 1-7, con propiedades anti proliferativas, anti inflamatorias, anti arrítmicas, y con efecto vasodilatador.
- Inflamación. El efecto de los inhibidores de SGLT2 sobre el sistema inflamatorio es desconocida. A nivel renal en modelos animales, existen datos sobre reducción de la expresión de marcadores de inflamación y estrés oxidativo; y más recientemente sobre célula beta, con reducción de apoptosis y especies reactivas de oxígeno (ROS)
La inhibición de SGLT2 reduce el hiperfiltrado glomerular. Diabetología 2017 Feb;60(2):215-225. Can J Diabetes 38 2014, 356-363.
La hiperglucemia es determinante para establecer la hiperfiltración y función hemodinámica en la diabetes, a través de la activación del SRAA (hipótesis neurohormonal para hiperfiltración), y efectos tubuloglomerulares (hipótesis tubular para hiperfiltración). Esto lleva a la glomeruloesclerosis y pérdida de la función renal. Por no poder medirse la filtración glomerular de cada nefrona en órganos intactos, los estudios en humanos utilizan medidas directas del GFR como subrogantes para presión intraglomerular.
Hipótesis neurohormonal para hiperfiltración
¿Qué causa hiperfiltración el DM tipo 1? La hiperglucemia aumenta la expresión génica y actividad de renina y angiotensina, resultando en vasoconstricción arteriolar eferente. Esto aumenta la presión intraglomerular, y por ende la hiperfiltración (que en humanos predice de manera independiente outcomes adversos como la microalbuminuria, insuficiencia renal e HTA). Se demostró que la inhibición de la ECA, reduce pero no normaliza la hiperfiltración en diabéticos tipo 1, por lo tanto su efecto protector es parcial.
Hipótesis tubular para hiperfiltración
La hiperglucemia relacionada a la diabetes aumenta la llegada de glucosa al TCP. Esto aumenta la reabsorción proximal de glucosa y Na+ por el aumento de la expresión y actividad de ARNm de SGLT2. A su vez, esto lleva a un descenso de Na+ en la mácula densa, lo que es sensado como un descenso del volumen circulante efectivo por el aparato yuxtaglomerular. Esto causa vasodilatación aferente, aumento de la presión intraglomerular e hiperfiltración, que conduce a nefropatía.
Se sugiere que la inhibición del SGLT2 reduce la hiperfiltración. Por lo tanto el inhibir este receptor, con o sin bloqueo del SRAA, tendría efectos beneficiosos.
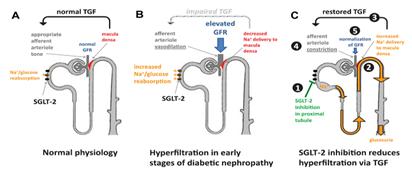
Figura 2. Feedback tubuloglomerular en fisiología normal y en DM no tratada que conduce a hiperfiltración, y mecanismo propuesto en DM con inhibición del SGLT2. (A) En condiciones fisiológicas, el feedback tubuloglomerular mantiene la tasa de filtrado glomerular (GFR) estable al modular el tono de la arteriola preglomerular. En condiciones de aumento de la GFR, la mácula densa en el aparato yuxtaglomerular sensa el incremento de la entrega de sodio distal y ajusta la GFR con el feedback tubuloglomerular. (B) Bajo hiperglucemia crónica (DM), el incremento en la reabsorción proximal de Na+ mediada por SGLT2 y glucosa altera este mecanismo de feedback. Así, a pesar del incremento en la GFR, la mácula densa queda expuesta a menor concentración de Na+. Esta alteración en el feedback posiblemente conduce a tono arteriolar indecuado y aumento de la perfusión renal. (C) La inhibición de SGLT2 con empagliflozin, bloquea la reabsorción proximal de glucosa y sodio, lo que conduce a incremento en el Na+ que llega a la mácula densa. Esto restaura el feedback tubuloglomerular controlando el tono arteriolar.
Efectos de la inhibición de SGLT2 sobre la función hemodinámica en diabetes
La inhibición del SGLT2 reduce de manera significativa la hiperfiltración renal en una proporción similar a la observada con la inhibición de la ECA. En ensayos clínicos con pacientes DM2 se observó que la inhibición del SGLT2 reduce el eGFR luego de 3 a 4 semanas de tratamiento, sugiriendo una disminución en la presión intraglomerular (similar a lo observado con los IECA). Este efecto es dosis dependiente, y está presente en pacientes con un amplio rango de eGFR (30 a 90 mL/min/1.73 m2). Este efecto sobre la inhibición de SGLT2 es reversible luego de 3 semanas.
Un reciente estudio a 8 semanas con empagliflozin redujo el filtrado glomerular un 19% en DM1. Este efecto fue independiente de la disminución o no en los niveles de glucosa. Canagliflozin en DM2 (con FG â¥55 ml/min) redujo el índice urinario albúmina:creatinina a 2 años, en comparación al grupo glimepirida.
Los inhibidores SGLT2 en diabéticos con insuficiencia renal
Las nefronas que sobreviven en estados avanzados de insuficiencia renal se asume que hiperfiltran para compensar la pérdida de otras nefronas. Como consecuencia, el efecto agudo en bajar el FG con los inhibidores del SGLT2 debería preservarse en la insuficiencia renal. Esto fue demostrado en DM2 con insuficiencia renal estadio 2 y 3, tratados con cana y empagliflozin. Al descenso modesto del eGFG se asoció una reducción en el índice urinario albúmina:creatinina.
El estudio EMPA-REG muestra evidencia que la combinación de los inhibidores SGLT2 con bloqueo de la angiotensina II proveen efectos nefroprotectores adicionales en DM2 con alto riesgo CV, incluyendo a aquellos con un FG de hasta 30 ml/min.
TRIALS ONGOING
- DECLARE (Dapagliflozin Effect on CardiovascuLAR Events).
- CANVAS (CANagliflozin CardioVascular Assessment Study).
- CREDENCE (Canagliflozin and Renal Events in Diabetes with Established Nephropathy Clinical Evaluation).
CONCLUSIONES
Los SGLT2i confieren un relativamente novedoso mecanismo de acción para reducir la glucemia. Se trata de fármacos ideales para ser combinados con metformina u otros antidiabéticos orales, obteniéndose resultados aditivos en reducir la glucemia y HbA1c (08 -1%). Presentan una baja incidencia de efectos adversos y una buena tolerancia oral. Se debe destacar que la hipoglucemia es casi inexistente, con la ventaja de ejercer su acción hipoglucemiante tanto en estadios de diabetes iniciales o avanzados (marcada insulinopenia), y de manera independiente del grado de insulinoresistencia. Como se ha comprobado recientemente, y tal como está ocurriendo con los análogos del GLP1 (estudio LEADER), estos fármacos tienen efectos beneficios adicionales sobre riñón y aparato cardiovascular (estudio EMPA-REG). Se están haciendo grandes esfuerzos en tratar de explicar cómo es que estos fármacos ejercen estos efectos pleiotrópicos. Finalmente, los SGLT2i escalan posiciones en el algoritmo de tratamiento de la DM2, siendo muy importantes en pacientes con patología cardiovascular. Al respecto, en las guías ADA 2017 y AACE 2017 se menciona que empagliflozin está indicado para reducir mortalidad cardiovascular en pacientes con DM2 y enfermedad cardiovascular. Debemos aguardar los nuevos datos de los estudios on-going.
Luego de la revisión de este tema hubo un comunicado el pasado 18 de mayo del 2017, donde la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés) alerta al público sobre los resultados de seguridad preliminares de un ensayo clínico aún en marcha en el que se descubrió un aumento en el número de amputaciones de pies y piernas, afectando sobre todo los dedos de los pies, en pacientes tratados con la medicina para la diabetes canagliflozina (Invokana, Invokamet). “No hemos determinado si la canagliflozina aumenta el riesgo de sufrir amputaciones de pies y piernas. Actualmente estamos investigando este nuevo problema de seguridad e informaremos al público en cuanto tengamos más información.” https://www.fda.gov/Drugs/DrugSafety/ucm502778.htm

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!