¿Hay riesgo de cáncer después del tratamiento con yodo radioactivo en el hipertiroidismo?
9 de enero 2020
Cancer Risk following Radioactive Iodine Treatment for Hyperthyroidism: a Cohort Study
Naomi Gronich et al. Thyroid, enero de 2020
Resumen:
Antecedentes: el yodo radioactivo se usa ampliamente para el tratamiento del hipertiroidismo. Los resultados de seguridad a largo plazo son limitados y contradictorios. Los objetivos de este estudio fueron evaluar la asociación del tratamiento con yodo radiactivo para el hipertiroidismo con el cáncer general y con tipos específicos de cáncer.
Métodos: Este es un estudio de cohorte histórico, que utilizó la base de datos de atención médica de Clalit, Haifa, Israel. Todos los participantes eran adultos con un reciente diagnóstico de hipertiroidismo en 2002 a 2015, recién tratados con yodo radioactivo o con tionamidas (propiltiouracilo/tiomazol), excluyendo pacientes con tumores malignos previos. La edad, el sexo, el historial de tabaquismo, el índice de masa corporal, el estado socioeconómico, el historial de diabetes mellitus y de hipertensión, el uso de aspirina y de estatinas, y el cumplimiento de los procedimientos de detección del cáncer se utilizaron para calcular el puntaje de propensión a recibir radioyodo. Se calcularon las tasas de incidencia y los intervalos de confianza del 95% para la aparición general de cáncer y para cada tipo de cáncer mediante la distribución de Poisson. La asociación entre las variables del estudio y el tiempo hasta el evento de cáncer se evaluó mediante razones de riesgo específicas de causa (HR) e intervalos de confianza (IC) del 95%. Para el análisis de sensibilidad, estratificamos la cohorte por año calendario al ingreso de la cohorte y por la duración del seguimiento.
Resultados: 16.637 pacientes formaron la cohorte del estudio, con 123.166 años-persona de seguimiento. No hubo asociación entre el tratamiento con yodo radiactivo y un mayor riesgo de cáncer en general HR = 0.99 (0.83-1.19, p = 0.91), HR = 1.01 (0.83-1.21, p = 0.95) (análisis univariados y multivariados, respectivamente). Sin embargo, en un análisis de sensibilidad, se encontró una asociación con el riesgo general de cáncer en el primer período de seguimiento (hasta 4,2 años) HR 2.11 (1.59-2.80) (p <0.0001), y ninguna asociación con un mayor riesgo en un período de seguimiento más largo.
En el análisis de riesgo univariado se encontró una asociación entre la exposición al radioyodo y un mayor riesgo de linfoma no Hodgkin (LNH), pero que no fue significativo en el análisis multivariado.
Conclusiones: no se encontró asociación entre el tratamiento con yodo radiactivo para el hipertiroidismo y el riesgo de cáncer incidente en el seguimiento a largo plazo. En un análisis de tipos de cáncer específicos, se encontró una asociación estadísticamente significativa con el LNH.
Comentario:
El yodo radioactivo (I131) se usa ampliamente para el tratamiento del hipertiroidismo resultante de la enfermedad de Graves, el adenoma tóxico y el bocio multinodular, y para el tratamiento del cáncer de tiroides. El radioyodo se incorpora a la glándula tiroides después de la administración oral, y su emisión beta daña el tejido y disminuye la función tiroidea. Otras medidas para disminuir la síntesis de las hormonas tiroideas en el hipertiroidismo son el tratamiento farmacológico con tionamidas y, con menos frecuencia, la cirugía.
Las guías de la Sociedad Americana de Tiroides (ATA por sus siglas en inglés) para el manejo de la Enfermedad de Graves recomiendan una dosis de yodo radioactivo suficiente para causar hipotiroidismo, típicamente de 10 a 15 mCi. Por lo general, se necesitan dosis de radioyodo ligeramente más altas para el tratamiento de adenomas tóxicos y bocios multinodulares, pero suelen ser más bajas que las utilizadas en el cáncer de tiroides (100-200 mCi).
Se ha planteado la preocupación por los posibles efectos cancerígenos del I131, exacerbada por los informes de una mayor incidencia de cánceres después de la exposición accidental a la explosión nuclear de Chernobyl, donde el principal isótopo contaminante fue I131; y un mayor riesgo de leucemia y de linfoma no Hodgkin (LNH) en los sobrevivientes de los bombardeos atómicos de Hiroshima y Nagasaki. En pacientes con cáncer de tiroides tratados con radioyodo, una actividad acumulativa creciente de I131 administrado se asocia con un mayor riesgo de cánceres sólidos y leucemia. En un análisis retrospectivo de pacientes con cáncer de tiroides, una dosis de I131 superior a 100 mCi se asoció con el riesgo de desarrollar leucemia, no así con dosis más bajas. Sin embargo, al estudiar pacientes con cáncer de tiroides tratados con radioyodo, la mayor incidencia de neoplasia maligna primaria secundaria también podría estar relacionada con una mayor vigilancia médica, lo que contribuye a una detección más temprana de los cánceres con una latencia prolongada, y también a factores etiológicos comunes a las dos neoplasias malignas, tales como factores hereditarios, así como a metástasis mal clasificadas.
Debido a que el hipertiroidismo tiene opciones alternativas de tratamiento además del radioyodo, es de suma importancia identificar el riesgo de cáncer asociado con su tratamiento.
Los datos sobre los resultados a largo plazo de pacientes tratados con I131 son limitados y contradictorios. Se ha observado un mayor riesgo de tipos específicos de cáncer, como de estómago, riñón y mama. Otros estudios informaron un aumento en la aparición de cáncer de tiroides solamente y una disminución en la incidencia general de cáncer.
En este trabajo se estudiaron todos los pacientes mayores de 18 años, con un reciente diagnóstico de hipertiroidismo (tirotoxicosis, bocio nodular tiroideo o neoplasia benigna de tiroides), entre enero de 2002 y junio de 2015 que fueron tratados con alguna tionamida (propiltiouracilo o tiamazol) o con yodo radioactivo. Si un paciente fue tratado con tioanamida y luego con yodo radiactivo, el tiempo se inició en la fecha de administración del radioyodo.
La cohorte para el análisis de la aparición de cáncer estuvo formada por 16.637 pacientes, con 123.166 años-persona (PY) de seguimiento. El tiempo medio de seguimiento fue de 7.27 años, (rango: 1-15 años). Hubo 2829 pacientes tratados con radioyodo. De ellos, 1808 fueron tratados con tionamidas seguido de radioyodo. 13.808 pacientes fueron tratados solo con tionamidas. La edad media de la cohorte fue de 51.9 (rango: 18-101) años. El 74% eran mujeres. A 2695 pacientes (95,3%) tratados con radioyodo se les administró solo una dosis de yodo radiactivo, 131 recibieron 2 dosis, 2 pacientes recibieron 3 dosis y 1 paciente recibió 4 dosis de yodo radiactivo.
825 pacientes fueron diagnosticados con cáncer incidente durante el seguimiento, lo que arroja una tasa general de cáncer incidente de 6.70 (IC 95% 6.26â7.17)/1000 PY de seguimiento. En los análisis de regresión de Cox, no se encontró asociación significativa entre el yodo radiactivo y el aumento del riesgo de cáncer en general. (Ver Fig 1 A)
Este estudio encontró una mayor ocurrencia de LNH en el pacientes expuestos a yodo radiactivo, con 7 casos entre 2829 expuestos a yodo radiactivo y 11 casos / 13.808 pacientes no expuestos a yodo radioactivo. El aumento de riesgo absoluto fue 2.18 / 1.000 PY (IC 95% â0.38â 4.68). (Ver Fig 1 B)
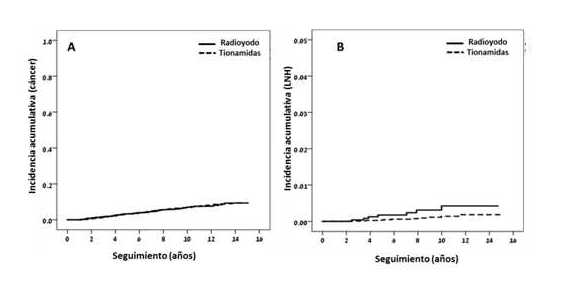
Fig 1: A: Incidencia acumulada de cáncer. B: Incidencia acumulada de LNH (Linfoma no Hodgkin)
De los 7 casos de LNH diagnosticados en el grupo de yodo radiactivo, 2 sufrieron LNH folicular en el cuello / tórax, 8 y 4 años después de la exposición; 4 fueron diagnosticados con linfoma de células B grandes en la cavidad abdominal / o LNH difuso entre 3 y 7 años después de la exposición; y 1 paciente fue diagnosticado con síndrome de Sezary 10 años después del tratamiento con yodo radiactivo.
En general, el tratamiento con tionamidas se asoció con una tasa de mortalidad más alta que el tratamiento con radioyodo.
El riesgo de cualquier cáncer asociado con la exposición a yodo radiactivo, aumentó en el primer período de seguimiento (hasta 4.2 años), y no se observó asociación con un mayor riesgo en pacientes seguidos durante 4.2 â8.9 años, así como tampoco en el seguimiento de más de 8.9 años.
El radioyodo puede causar daño a la médula ósea, dando lugar a aberraciones cromosómicas y, finalmente, a la transformación maligna. Se encontraron daños cromosómicos agudos y tardíos en linfocitos periféricos de pacientes que recibieron varias dosis de I131, con una mayor tasa de recuperación en los pacientes con tirotoxicosis. El efecto leucemogénico de la radiación tiene un período latente de al menos dos años, mientras que los efectos tumorigénicos informados en los órganos sólidos requieren más años.
En una cohorte de 308.297 trabajadores monitoreados por radiación, la mayor asociación fue entre la dosis acumulativa de radiación ionizante y la muerte causada por la leucemia mieloide crónica, pero también hubo una asociación con la mortalidad por LNH y otras neoplasias hematológicas. Los informes de la asociación entre el yodo radioactivo para el hipertiroidismo y el cáncer son inconsistentes.
En el Estudio Cooperativo de Seguimiento de la Terapia de Tirotoxicosis, la terapia con yodo radiactivo no se relacionó con la mortalidad general por cáncer ni con la mortalidad por ningún cáncer específico, después de excluir a los pacientes tratados quirúrgicamente y con tumores malignos anteriores. Por el contrario, un estudio finlandés en 2793 pacientes, y sus controles de la población por edad y sexo, mostró que la incidencia general de cáncer fue mayor entre los pacientes que en los controles. El riesgo de cánceres de estómago, riñón, mama y sitio no especificado se incrementó. Debido a que el grupo de control en este estudio eran sujetos de la población general, podrían haber estado bajo controles de salud menos rigurosos y, por lo tanto, el sesgo de detección podría haber influido en los resultados.
Un seguimiento extendido recientemente publicado sobre 18.805 pacientes del Estudio Cooperativo de Seguimiento de la Terapia de Tirotoxicosis, tratado entre 1946-1964, confirmó una relación dosis-respuesta, al mostrar una asociación entre la actividad calculada de I131 absorbida por cada órgano y los resultados de mortalidad por cánceres sólidos. Un mínimo exceso de riesgo de mortalidad, en comparación con la población general, ocurrió en los primeros 20 años después del tratamiento. No hubo asociación dosis-respuesta con la muerte por cáncer de tiroides, a pesar de las altas actividades calculadas recibidas por la tiroides.
En el estudio presentado aquí, observamos una incidencia global de cáncer de 6.70 (6.26â7.17) casos / 1000 PY de seguimiento, similar a las tasas informadas en otros países occidentales. Hemos observado una disminución del riesgo de cáncer de tiroides asociado con el radioyodo, en comparación con el riesgo asociado con las tionamidas. Debido a que los tirocitos son atacados y destruidos por el radioyodo, especulamos que esto puede resultar en una disminución en la incidencia de cáncer de tiroides bien diferenciado.
Las limitaciones de este estudio son, en primer lugar la posibilidad de un sesgo diferencial, ya que los médicos podrían haber recomendado el tratamiento con yodo radioactivo a pacientes de mayor edad con más frecuencia que la recomendación de tionamidas. En segundo lugar, podría haber ocurrido un sesgo de detección, porque los pacientes tratados solo con tionamidas requirieron un seguimiento endocrinológico más cercano ya que el estado de hipertiroidismo no se curó como en el grupo de yodo radioactivo. Además, un seguimiento más cercano podría haber detectado casos de cáncer oculto. El cáncer de tiroides es un excelente ejemplo para el cual la vigilancia intensificada podría haber resultado en una mayor incidencia de cánceres tempranos con comportamiento indolente (sobre-diagnóstico). Este sesgo de sobre-diagnóstico tenderá a aumentar la detección de cáncer en nuestro grupo de control y, por lo tanto, afectará la disminución del riesgo observado en asociación con el yodo radioactivo. La tercera limitación es la falta de cuantificación de los mCi de cada dosis recibida por los pacientes. La cuarta limitación se relaciona con la incidencia de cánceres específicos en Israel. El cáncer de estómago, por ejemplo, tiene una amplia variación geográfica en todo el mundo. Israel, tiene una de las tasas más bajas. Debido al pequeño número de casos de cáncer de estómago encontrados en Israel, podría haberse producido un error aleatorio en nuestro estudio al evaluar una posible asociación de cáncer de estómago con radioyodo.
En conclusión, en este estudio de cohorte se pudo observar que el tratamiento con radioyodo para el hipertiroidismo no está asociado con un mayor riesgo de cáncer en general. Sin embargo, puede haber una asociación con un mayor riesgo de LNH. Estudios prospectivos pueden estar justificados para confirmar los resultados.
Copyright 2020. Endoweb.net
<div style="width: 100%;"><div style="position: relative; padding-bottom: 56.25%; padding-top: 0; height: 0;"><iframe frameborder="0" width="1200" height="675" style="position: absolute; top: 0; left: 0; width: 100%; height: 100%;" src="https://view.genial.ly/5e57d7ff2cf4060fd265c8e5" type="text/html" allowscriptaccess="always" allowfullscreen="true" scrolling="yes" allownetworking="all"></iframe> </div> </div><

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!