¿Cuándo dar zoledronato post denosumab?
16 de julio 2020
Treatment with zoledronate subsequent to denosumab in osteoporosis: a randomized trial
Anne Sophie Sølling, Torben Harsløf and Bente Langdahl. Journal of Bone and Mineral Research|May 29, 2020
Tratamiento con zoledronato posterior a denosumab en osteoporosis: un ensayo aleatorizado
RESUMEN
Debido a que la suspensión de denosumab se asocia con pérdida ósea y posiblemente un mayor riesgo de fractura, en este estudio se investigó si el tratamiento con zoledronato podría prevenir la pérdida ósea y si el momento de la infusión de zoledronato influyó en el resultado.
Se trata de un estudio intervencionista aleatorizado, abierto, de 2 años de duración, que incluyó a 61 pacientes con osteopenia, que suspendieron denosumab después de 4.6 ± 1.6 años. Se administró zoledronato seis meses (grupo 6M, n = 20) o nueve meses (grupo 9M, n = 20) después de la última inyección de denosumab o cuando el recambio óseo había aumentado (grupo OBS, n = 21). Se controló a los pacientes con DXA y marcadores de recambio óseo. Los objetivos primarios fueron el cambio en la DMO de la columna lumbar seis meses después del zoledronato y la proporción de pacientes que no pudieron mantener la DMO. El estudio continúa en curso (clinictrials.gov NCT03087851).
59 pacientes, de 61 incluidos, completaron el seguimiento de 12 meses después del zoledronato. La DMO columna lumbar disminuyó significativamente en 2.1 ± 0.9% (media ± SEM), 4.3 ± 1.1% y 3.0 ± 1.1% a los 6 meses después del zoledronato en los grupos 6M, 9M y OBS, respectivamente, y en 4.8 ± 0.7%, 4.1 ± 1.1%, y 4.7 ± 1.2% a los 12 meses del zoledronato en los grupos 6M, 9M y OBS, respectivamente (p <0.02, sin diferencias entre los grupos). La pérdida de DMO por encima del mínimo cambio significativo se observó en todos los grupos; en columna lumbar: 6M: n = 6 (30%), 9M: n = 9 (45%), OBS: n = 9 (47%); y en la cadera total: 6M: n = 1 (5%), 9M: n = 5 (25%), OBS: n = 2 (11%). En el grupo 6M, el telopéptido C-terminal (CTX) disminuyó inicialmente, pero aumentó rápidamente a partir de entonces, y seis meses después de zoledronato. El CTX aumentó rápidamente en los grupos 9M y OBS, fue suprimido por zoledronato, pero aumentó nuevamente a partir de entonces. Se observaron fracturas vertebrales incidentales en dos mujeres del grupo 9M.
Conclusión: El tratamiento con zoledronato, independientemente del momento, no pudo prevenir por completo la pérdida de la DMO en pacientes que discontinuaron denosumab.
INTRODUCCIÃN
La terapia a largo plazo con denosumab (DMAB) por hasta diez años aumenta progresivamente la densidad mineral ósea (DMO) tanto en la columna lumbar (CL) como en la cadera total (CT) y disminuye de manera persistente el riesgo de fractura. Sin embargo, cuando se suspende el tratamiento, el recambio óseo aumenta rápidamente y la masa ósea que se ganó durante el tratamiento, se pierde en 12-24 meses. Además, el riesgo de fracturas vertebrales asociadas al “rebote” del recambio óseo, puede aumentar durante la fase de pérdida ósea rápida.
Es por esto que no se recomienda suspender el tratamiento con DMAB. Sin embargo, algunos pacientes mejoran su DMO y muestran osteopenia o incluso DMO normal durante el tratamiento y cumplen los criterios establecidos para la interrupción de la terapia. Se ha demostrado que el riesgo de fracturas no vertebrales (NVFx) disminuye con el aumento de la DMO y que este riesgo no disminuye aún más una vez que la DMO de cadera alcanza un T score de -1.5, por lo que sería interesante poder suspender DMAB cuando se alcanza la mejoría deseada.
El zoledronato (ZOL) es un bifosfonato con efecto antirresortivo, que a diferencia del DMAB, su efecto se mantiene durante años después de su interrupción. Una serie de casos en mujeres que habían sido tratadas con DMAB durante siete años en el estudio FREEDOM, mostró que una infusión de ZOL posterior a la suspensión del DMAB no previno la pérdida ósea. Los autores especularon que esto pudo deberse a que el recambio óseo aún estaba suprimido en el momento de la administración de ZOL.
El objetivo de este ensayo clínico es investigar si el tratamiento con ZOL podría prevenir aumentos en el recambio óseo y la pérdida de la densidad mineral ósea, en pacientes tratados previamente con DMAB, y también si el efecto de ZOL depende del momento de la administración después de la última inyección de DMAB.
Los endpoints primarios fueron el cambio en la DMO de CL desde el inicio hasta seis meses después de ZOL y la proporción de pacientes que no pudieron mantener la DMO.
Los endpoints secundarios fueron los cambios en los marcadores óseos, DMO y el score de hueso trabecular (TBS) desde el inicio hasta los 6 y 12 meses después de ZOL, y fractura vertebral (VFx) morfométrica un año después de la primera infusión de ZOL.
En esta publicación se presentan los resultados de los primeros 12 meses después de la administración inicial de ZOL.
DISEÃO
Se realizó un estudio aleatorizado, abierto, de intervención, en 61 pacientes.
Los participantes fueron asignados al azar 1: 1: 1 en tres grupos para recibir ZOL:
1. Grupo 6M: seis meses después de la última aplicación de DMAB (cuando se debería haber administrado el próximo DMAB)
2. Grupo 9M: nueve meses después de la última aplicación de DMAB (donde se esperaría que el recambio óseo fuera alto según los estudios de interrupción anteriores)
3. Grupo OBS: un grupo de observación que recibió el ZOL cuando los CTX aumentaron por encima de 1.26 μg/l (50% por encima del rango normal para mujeres posmenopáusicas y hombres de edad avanzada).
Se incluyeron mujeres posmenopáusicas (posmenopáusicas durante al menos dos años) y hombres mayores de 50 años, que recibieron DMAB durante al menos dos años antes del inicio del estudio.
Se excluyeron pacientes con fractura vertebral, o de cadera en los últimos 12 meses, T score <-2.5 en CL o CT, tratamiento en curso con glucocorticoides sistémicos, enfermedad metabólica ósea, terapia de reemplazo hormonal, cáncer, TFGe <35 ml/min, hipocalcemia, contraindicaciones para ZOL, y el tratamiento con alendronato durante más de tres años. No se excluyeron pacientes tratados con otros bifosfatos durante más de tres años.
El tratamiento consistió en una infusión intravenosa de 5 mg de ZOL. Se aseguró una ingesta diaria de 1000 mg de calcio y 38 ug de vitamina D mediante suplementos.
El grupo 6M recibió ZOL al inicio del estudio (6 meses después de la última inyección de DMAB) y el grupo 9M al tercer mes de inicio del estudio (9 meses después del último DMAB) (con una ventana de tratamiento ± 14 días). Sin embargo, como precaución, para el grupo 9M, si el CTX aumentó por encima de 1.26 μg/l en el mes 1 o 2 post inicio del estudio, se administró ZOL en ese momento. Además, si un paciente tuvo una fractura vertebral o de cadera, la infusión de ZOL se administró en ese momento. En el grupo OBS, se administró ZOL si el CTX aumentó por encima de 1.26 μg/l (monitorizado mensualmente), la DMO disminuyó más del 5% en CL o CT, o si un paciente tuvo una fractura vertebral o de cadera; y se administró ZOL a más tardar a los 6 meses.
Toda la población de estudio se controló luego de la primera infusión con ZOL con marcadores óseos en los meses 1 y 2 post ZOL (grupos 9M y OBS solamente) o mes 3 post ZOL (grupo 6M), y todos los grupos en los meses 6 y 12, y con DXA en los meses 6 y 12 post ZOL.
En todos los casos, se administró una infusión adicional de ZOL si CTX aumentó por encima de 1.26 μg/l, o si la DMO disminuyó más del 5% en CT o CL.
RESULTADOS
DMO
Desde el inicio del estudio hasta 6 meses después de ZOL, la DMO de CL disminuyó significativamente en 2.1 ± 0.9%, 4.3 ± 1.1% y 3.0 ± 1.1%; y a los 12 meses después de ZOL en 4.8 ± 0.7%, 4.1 ± 1.1 % y 4.7 ± 1.2% en los grupos de 6M, 9M y OBS, respectivamente (p <0.02, sin diferencias entre los grupos). De manera similar, la DMO de CT disminuyó significativamente en 1.3 ± 0.5%, 2.7 ± 0.8%, 2.3 ± 0.6% desde el inicio hasta 6 meses después de ZOL; y en 2.6 ± 0.5%, 3.2 ± 0.8%, y 3.6 ± 0.8% desde el inicio hasta 12 meses después ZOL en los grupos de 6M, 9M y OBS, respectivamente (p <0.02, sin diferencias entre los grupos). En el cuello femoral, la DMO disminuyó en 1.3 ± 0.5%, 4.2 ± 1.0%, 2.7 ± 0.7% desde el inicio hasta seis meses después de ZOL en los grupos 6M, 9M y OBS, respectivamente; y en 3.0 ± 0.5%, 3.5 ± 1.0% y 4.6 ± 1.0% desde el inicio hasta 12 meses después de ZOL en 6M, 9M y OBS, respectivamente (pâ¤0.002, sin diferencias entre grupos). El TBS disminuyó en el grupo 9M desde el inicio hasta los 12 meses después de ZOL (2.9 ± 0.68%, p = 0.003).
No hubo diferencia en el cambio porcentual medio en la DMO en ningún momento entre los tratados con bifosfonatos antes de DMAB, y los que no recibieron bifosfonatos previamente.
Figura 1. Porcentaje de cambio medio en la DMO de columna lumbar durante el estudio en los 3 grupos de tratamiento
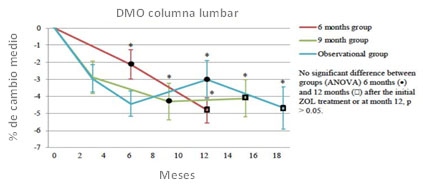
Figura 2. Porcentaje de cambio medio en la DMO de cadera total durante el estudio en los 3 grupos de tratamiento
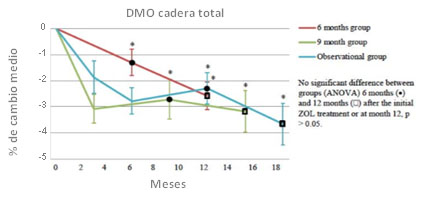
MARCADORES ÃSEOS
Todos los marcadores óseos medidos, aumentaron significativamente desde el inicio hasta los 6 y 12 meses después de ZOL. Después del tratamiento con ZOL en el grupo 6M, los CTX disminuyeron por debajo de los niveles basales en el mes 1 (p <0.001), pero aumentaron nuevamente en los meses 3, 6 y 12 (p <0.001 para todos), y alcanzaron niveles máximos por encima del intervalo de referencia para mujeres pre menopáusicas, a los 6 meses. En comparación con la línea de base, PINP y osteocalcina aumentaron significativamente a los 6 y 12 meses (p <0.001 para ambos), y alcanzaron valores máximos al mes 12.
En el grupo 9M, los CTX aumentaron rápidamente por encima del rango de referencia pre menopáusico al mes 2 y 3 del inicio del estudio (p <0.001 para ambos) y, luego de la infusión de ZOL disminuyeron hacia el valor basal en el mes 1 (p <0.001), pero aumentaron nuevamente a partir de entonces hacia los meses 6 y 12 (p <0.001 para ambos). PINP y osteocalcina mostraron patrones similares, aunque los valores medios permanecieron dentro del rango de referencia pre menopáusico.
En el grupo OBS, hubo un rápido aumento en los CTX desde el inicio del estudio hasta los meses 2, 3, 4, y 6 (máximo en el mes 6), con valores por encima del rango de referencia pre menopáusico. Después de ZOL, los CTX disminuyeron por debajo de los valores basales (p <0.001), pero aumentaron nuevamente a partir de entonces.
El aumento en los CTX a los meses 6 (p = 0.045) y 12 (p = 0.020) después de ZOL fue mayor en el grupo 6M en comparación con los otros grupos.
El aumento de osteocalcina fue mayor en el grupo 6M después de 12 meses, en comparación con los otros dos grupos (p = 0.002). Al comparar los cambios desde el inicio hasta los 12 meses no hubo diferencias entre los grupos para CTX o PINP, pero la osteocalcina aumentó más en el grupo 6M (p = 0.043).
No hubo diferencias en el cambio porcentual medio en ninguno de los marcadores 12 meses después de la primera infusión de ZOL, entre los tratados y no tratados con bifosfonatos antes de DMAB.
Figura 3. Valor de CTX durante el estudio en los 3 grupos de tratamiento
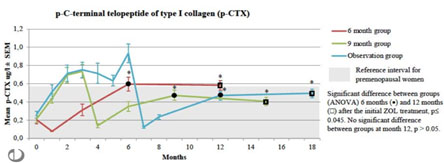
Correlaciones
La duración del tratamiento con DMAB se correlacionó significativamente con los CTX basales (p = 0.029). Se encontró CTX basal significativamente más alto en pacientes que habían sido tratados con DMAB ⥠mediana (5.0 ± 3.5 - 6 años (mediana ± IQR)).
Además, la duración del tratamiento con DMAB se correlacionó con el cambio en la DMO de CF 6 meses después de ZOL (p = 0.006) y en CL 12 meses después de ZOL (p = 0.003). Hubo una mayor pérdida de la DMO en pacientes con duración del tratamiento con DMAB ⥠mediana. Además, se encontró que tanto el CTX basal como la edad, se correlacionaron con el cambio porcentual medio en la DMO de CT 6 y 12 meses después de ZOL (p⤠0.044 para ambos).
Efectos adversos
Casi el 61% de los pacientes experimentó síntomas similares a la gripe después del tratamiento inicial con ZOL. No se observaron casos de osteonecrosis de la mandíbula o fractura femoral atípica.
Cuatro pacientes sufrieron una fractura durante el seguimiento: húmero (fractura traumática, grupo 6M, en el mes 9 post ZOL), costilla (grupo OBS, en mes 10 post ZOL), L1 sintomático (grupo 9M, en mes 9 post ZOL) y L1 sintomático (grupo 9M, 9 meses post ZOL).
DISCUSIÃN
Este estudio aún en curso, informa los resultados desde el inicio hasta los 12 meses posteriores al tratamiento inicial con ZOL. Se observó que una infusión de ZOL no fue suficiente para mantener la supresión de los marcadores óseos y prevenir completamente la pérdida ósea en cualquier grupo. En el grupo 6M, los CTX fueron suprimidos por ZOL, por lo tanto, se evitaron niveles muy altos de CTX y una pérdida ósea rápida, lo cual es atractivo desde un punto de vista clínico, ya que el alto recambio óseo está asociado con la pérdida de hueso trabecular y riesgo de fracturas. Sin embargo, en este grupo, el 50% de los pacientes necesitaron un nuevo tratamiento con ZOL de acuerdo con los criterios especificados en el protocolo del estudio.
Se ha demostrado previamente que algunos pacientes han suprimido los marcadores casi por completo seis meses después de la última inyección de DMAB, pero también que la mayoría ha recuperado cierta actividad de resorción ósea tres meses después.
Se investigaron diferentes puntos de tiempo para la infusión de ZOL, ya que se ha especulado que, si el remodelado óseo es fuertemente suprimido por la inyección previa de DMAB, ZOL puede no adherirse lo suficiente a la superficie del hueso para inhibir la reactivación de la resorción una vez que el efecto de DMAB desaparezca. También se investigó el efecto de ZOL cuando los CTX alcanzaron un nivel alto (grupo OBS), eligiendo como valor de corte 50% superior al rango normal para mujeres posmenopáusicas y hombres de edad avanzada.
Un análisis post hoc del ensayo FREEDOM encontró una menor incidencia de NVFx con T scores de cadera más altos, que fue independiente de la frecuencia y las VFx prevalentes. Sin embargo, cuando los T score fueron mayores a -1.5, el riesgo de NVFx no disminuyó aún más, lo que sugiere que un T score de cadera ⥠-1.5 podría ser un objetivo de tratamiento apropiado en la práctica clínica.
Se han investigado diferentes estrategias para mantener la DMO en pacientes previamente tratados con DMAB. En el estudio DAPS, un grupo de mujeres posmenopáusicas fueron aleatorizadas a recibir ALN 70 mg/semana vs DMAB 60 mg/6 meses durante un año, y luego cambiaron a DMAB o ALN durante el segundo año. En este estudio, de corto plazo de tratamiento con DMAB, luego de su suspensión, ALN preservó la DMO en la columna lumbar y la cadera.
En una serie de casos, Horne y col. descubrieron que las ganancias de la DMO obtenidas durante el tratamiento con romosozumab durante un año y DMAB durante dos años (estudio FRAME) se mantuvieron en el 73-87% de los pacientes 12 meses después de recibir una infusión de ZOL a los 8 meses (mediana), después de suspender el DMAB. Sin embargo, 24 meses después de ZOL, la DMO de CL y cadera habían disminuido. Lehmann y col, presentaron otra serie de casos con 22 mujeres posmenopáusicas tratadas con una sola infusión de ZOL después de dos años de tratamiento con DMAB. Aproximadamente el 33% de la masa ósea lograda en CL con DMAB, se perdió cuando se midió 2.5 años después de ZOL. Reid y sus colegas demostraron una disminución significativa en la DMO en CL y CT en seis mujeres posmenopáusicas tratadas con ZOL 6 meses después de suspender el DMAB luego de recibirlo por siete años. Un estudio observacional que incluyó a 120 mujeres posmenopáusicas tratadas con DMAB durante 2-3 años, recibieron una única infusión de ZOL 6 meses después de la última inyección de DMAB. Entre 6 a 36 meses después del tratamiento con ZOL la DMO había disminuido significativamente en un 3.3% en CL, 2.2% CT y 1.5% CF. Los CTX y PINP medidos en un subgrupo (n = 27) en el mismo punto de tiempo, estaban dentro del rango de referencia. Anastasilakis y col, realizaron un ensayo clínico (AfterDmab) con 57 mujeres posmenopáusicas tratadas con DMAB durante 2-2.4 años, aleatorizadas a recibir dos inyecciones de DMAB 60 mg/6 meses o una sola infusión de ZOL 5 mg. En este estudio, a diferencia de los estudios mencionados previamente, se informó un aumento de la DMO de CL después de 12 meses (+ 1.7%), pero una disminución de la DMO hacia los valores basales después de 24 meses (0.1%) en las mujeres tratadas con ZOL, y un patrón similar para la DMO de CT. Tanto PINP como CTX aumentaron en el mes 24 en comparación con los niveles basales.
Al comparar los resultados del trabajo actual que aquí se resume, con el ensayo AfterDmab y el estudio observacional, parece importante discutir algunas diferencias.
Los datos del estudio observacional no se recopilaron de manera estandarizada y solo incluyen marcadores óseos en un pequeño subgrupo de pacientes. Estos estudios solo incluyeron mujeres posmenopáusicas, mientras que en el estudio actual incluyó a hombres y mujeres (87% mujeres) con una edad media ligeramente más alta (67.7 años vs. 65.2 y 65.6 años) y probablemente lo más importante, una mayor duración del tratamiento con DMAB (4.6 ± 0.2 años vs. 2.4 ± 0.2 años y 2-3 años).
Los diferentes resultados de los estudios sugieren que la duración del tratamiento con DMAB es un factor importante para determinar si una infusión de ZOL es suficiente para mantener la supresión de los marcadores y evitar así la pérdida ósea después de la interrupción del DMAB. En el caso de un tratamiento a corto plazo con DMAB, como en el estudio DAPS y el ensayo AfterDmab, el incremento de la osteoclastogénesis tras la interrupción de DMAB podría no ser tan fuerte como el observado con una mayor duración del tratamiento y, por lo tanto, puede explicar por qué los bifosfonatos fueron capaces de preservar la DMO. Otra indicación de que la duración del tratamiento con DMAB desempeña un papel importante proviene de la serie de casos extendida que demostró que aquellos con tratamiento con DMAB por menos de dos años tendieron a tener menos VFx (⤠2 años: 3.2 ± 0.7 vs 5.2 ± 1.4, p < 0.055).
El presente trabajo apoya la sugerencia de que la duración del tratamiento con DMAB es importante.
Los autores encontraron que el CTX basal fue mayor en pacientes que habían sido tratados por un período más largo con DMAB. Esta menor supresión de la resorción ósea con la duración del tratamiento también se observó en el estudio FREEDOM y se ha atribuido a mecanismos contrarreguladores en respuesta a la supresión prolongada del recambio óseo. Los mecanismos subyacentes no se entienden completamente, pero se sospecha que un aumento compensatorio de la producción de RANKL y la acumulación de preosteoclastos son factores importantes. También encontraron que el CTX basal, la duración del tratamiento con DMAB y la edad influyeron en el resultado. Estas interacciones se observaron con mayor claridad en el grupo 9M donde se produjo una pérdida ósea rápida entre el inicio del estudio y la infusión de ZOL y más rápidamente en las mujeres con CTX por encima del valor medio. Estos efectos se observaron predominantemente en los sitios de la cadera, lo que subraya la importancia de la DMO de cadera y los cambios en la DMO en esta región, como también lo demostró recientemente el proyecto de calidad ósea del FNIH (Eastell R, et al. FNIH Bone Quality Project. 2019 Abstr. - Am. Soc. Bone Miner. Res., 2009).
Hasta la fecha, este ensayo clínico aleatorizado es el estudio más grande para abordar la pérdida ósea después de la interrupción de DMAB. Las características basales estuvieron bien equilibradas entre los grupos de tratamiento, y hubo muy pocos abandonos durante todo el ensayo. El hecho de que se incluyeran tanto hombres como mujeres y, pacientes con o sin tratamiento previo para fracturas, refleja la práctica clínica y mejora la validez externa de los resultados. Los marcadores de recambio óseo se midieron con frecuencia permitiendo una mejor comprensión de los mecanismos subyacentes. Los autores destacan que cuando se diseñó el estudio, tuvieron en cuenta los reportes sobre el aumento de los marcados óseos y pérdida de la DMO, así como también el mayor riesgo de VFx. Por lo que decidieron, como medida de seguridad, que los pacientes con niveles muy altos de CTX o una fractura por fragilidad, recibieran ZOL.
Las limitaciones de este estudio incluyen el diseño de etiqueta abierta, ninguna evaluación por VFA o rayos X de VFx al inicio, y los cambios en el tratamiento que no están de acuerdo con el protocolo (n = 6 cambiaron de ZOL a DMAB, n = 1 no cumplió con el criterio de CTX o de DMO, n = 1 comenzó ZOL 4 mg cada 6 meses). La información sobre DMO antes del inicio de DMAB no está disponible y, por lo tanto, la pérdida de la DMO no puede evaluarse en el contexto de la ganancia densitométrica durante el tratamiento con DMAB. El límite de CTX fue 50% superior al rango normal para mujeres posmenopáusicas y hombres de edad avanzada, y no se puede descartar que el resultado del estudio hubiera sido diferente con un límite distinto.
Conclusión
En pacientes que suspenden DMAB después del tratamiento a largo plazo, una sola infusión intravenosa de ZOL 5 mg administrada seis o nueve meses después de la última inyección de DMAB, o cuando se incrementa el recambio óseo, no es suficiente para prevenir por completo la pérdida ósea.
Independientemente de la estrategia, debe esperarse una pérdida promedio de la DMO de 0.25-0.5 desvíos standard y, por lo tanto, la DMO probablemente sea más alta que la DMO objetivo para la interrupción del tratamiento con bifosfonato, al considerar la interrupción de DMAB.
Según el grupo 6M, donde se evitaron niveles muy altos de CTX y una pérdida ósea rápida, el tratamiento con ZOL seis meses después de la última inyección de DMAB, parece ser la opción más atractiva de las investigadas en este trabajo. Pero basado en el rápido aumento de los CTX después de la disminución inicial en el grupo 6M, los autores especulan que algunos pacientes se beneficiarían de una segunda infusión de ZOL 3-6 meses después, sin embargo, esto debe investigarse en un ensayo clínico. Dependiendo del acceso a la medición de los marcadores óseos, diferentes estrategias pueden ser preferibles en la práctica clínica.
Copyright 2020. Endoweb.net

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!