¿COVID-19 puede producir tirotoxicosis?
20 de octubre 2020
Tirotoxicosis en pacientes con COVID-19: estudio THYRCOV
Thyrotoxicosis in patients with COVID-19: the THYRCOV study. Andrea Lania, Maria Teresa Sandri, Miriam Cellini , Marco Mirani , Elisabetta Lavezzi , Gherardo Mazziotti. Eur J Endocrinol. 2020 Oct;183(4):381-387. doi: 10.1530/EJE-20-0335.
Resumen:
Objetivo: Este estudio evaluó la función tiroidea en pacientes afectados por la enfermedad por coronavirus-19 (COVID-19), basado en la hipótesis de que la tormenta de citokinas asociada con COVID-19 puede influir en la función tiroidea; y/o el síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2) puede actuar directamente sobre las células tiroideas, como se demostró anteriormente para la infección por SARS-CoV-1.
Diseño y métodos: Este estudio fue retrospectivo, en un único centro, y consistió en evaluar las pruebas de función tiroidea y los valores séricos de interleucina-6 (IL-6) en 287 pacientes consecutivos (193 hombres, mediana de edad: 66 años, rango: 27-92) hospitalizados por COVID-19 en unidades de cuidados no intensivos.
Resultados: Se encontraron 58 pacientes (20,2%) con tirotoxicosis (manifiesta en 31 casos), 15 (5,2%) con hipotiroidismo (manifiesta en solo 2 casos) y 214 (74,6%) con función tiroidea normal. Los valores de tirotrofina sérica (TSH) se correlacionaron inversamente con la edad de los pacientes (0,27; P < 0,001)y con los valores de IL-6 (0,41; P < 0,001). En el análisis multivariado, la tirotoxicosis resultó estar asociada en forma significativa con una IL-6 más alta (razón de probabilidades: 3,25, intervalo de confianza del 95%: 1,97–5,36; P < 0,001).
Conclusiones: Este estudio proporciona la primera evidencia de que COVID-19 puede estar asociado con un alto riesgo de tirotoxicosis en relación con la activación inmune sistémica inducida por la infección por SARS-CoV-2.
Comentario:
El síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2) es un nuevo coronavirus responsable de la enfermedad por coronavirus-19 (COVID-19) que va desde casos asintomáticos hasta afectación respiratoria grave. El primer caso clínico de COVID-19 en Italia fue diagnosticado el 20 de febrero de 2020; entonces la infección se ha extendido rápidamente.
Un subgrupo de pacientes graves con COVID-19 podría tener una tormenta de citokinas caracterizada por hiperactividad de respuesta inmune, con aumento de la producción de varias citokinas proinflamatorias, incluida la interleucina 6 (IL-6) y el factor de necrosis tumoral alfa (TNF-α). El patrón de citokinas observado en pacientes con COVID-19 es similar al que ocurre en algunas enfermedades reumatológicas o durante inmunoterapias para el cáncer. Además, la respuesta de citokinas descrita en COVID-19 es similar, al menos en parte, a la activación inmunitaria que acompaña a las enfermedades inflamatorias de la tiroides. Específicamente, se describió una hiperactivación de la respuesta Th1 en linfocitos periféricos en pacientes con tiroiditis autoinmune e inducida por fármacos y se informó un aumento de IL-6 en el curso de la tiroiditis destructiva. De hecho, se informaron alteraciones de la función y estructura de la tiroides en pacientes afectados por SARS-CoV-1, pero los mecanismos no fueron aclarados y aún se desconoce si una afectación similar puede ocurrir también durante el COVID-19, como consecuencia de los efectos directos o indirectos del virus en la glándula tiroides.
En este estudio retrospectivo, el objetivo fue investigar la prevalencia y los determinantes de la función tiroidea alterada en pacientes hospitalizados por COVID-19. Fue realizado en 287 pacientes consecutivos hospitalizados por COVID-19 en el Centro de Investigación y Clínica Humanitas IRCCS, Rozzano-Milán, Italia, en el período comprendido entre el 1 de marzo y el 1 de abril de 2020. Los criterios de inclusión fueron (i) hospitalización por COVID-19 diagnosticado mediante PCR-RT de muestras de frotis nasal y faríngeo o líquido de lavado broncoalveolar asociado con signos clínicos y radiológicos de neumonía, y (ii) al menos una medición de tirotropina sérica (TSH) después del diagnóstico de COVID-19. Los criterios de exclusión fueron (i) tratamiento con Levotiroxina o fármacos antitiroideos antes y en el momento de la evaluación de TSH; (ii) tratamiento con amiodarona; (iii) inicio de inmunoterapia antes de la medición de los valores de TSH; y (iv) requerimiento de intubación y soporte respiratorio mecánico en el momento de la evaluación de TSH.
La medición de TSH se incluyó en la evaluación bioquímica de rutina de los pacientes hospitalizados con COVID-19. En pacientes con valores de TSH en suero por debajo o por encima del rango de referencia, se midieron tiroxina libre (FT4) y triyodotironina libre (FT3) para una evaluación integral de la función tiroidea. En algunos pacientes con tirotoxicosis manifiesta, se realizaron ecografías de tiroides y mediciones de anticuerpos contra el receptor de TSH (TRAb), anticuerpos antitiroglobulina (TgAc) y anticuerpos antitiroperoxidasa (TPOAc). La función tiroidea se evaluó el primer día de hospitalización con muestras de sangre extraídas en ayunas.
Cincuenta y ocho pacientes (20,2%) mostraron TSH por debajo del rango de referencia (<0,10 mU/L en 16 casos, entre 0,10 y 0,33 mU/L en 42 casos), mientras que la TSH fue normal y alta en los 214 (74,6%) y 15 (5,2%) pacientes restantes, respectivamente. En 214 pacientes con valores de TSH en el rango de referencia, 99 (46,3%) tenían valores entre 0,34 y 1,0 mU/L.
Se obtuvieron el resto de las valoraciones tiroideas en 73 pacientes con valores anormales de TSH. Se diagnosticó disfunción tiroidea manifiesta en 33 pacientes (31 con tirotoxicosis y 2 con hipotiroidismo), mientras que 40 pacientes (27 con tirotoxicosis y 13 con hipotiroidismo) presentaron una disfunción tiroidea subclínica. Antes de la evaluación de la función tiroidea, 30 pacientes con tirotoxicosis (51,7%) recibieron tromboprofilaxis con heparina de bajo peso molecular (P = 0,39 vs pacientes sin tirotoxicosis) y a 3 pacientes (5,2%) les habían realizado Tomografía computarizada torácica con contraste yodado (P = 0,17 frente a pacientes sin tirotoxicosis).
Los pacientes con tirotoxicosis manifiesta mostraron valores de FT4 séricos más altos en comparación con aquellos con tirotoxicosis subclínica, sin significante diferencia en los valores de FT3 en suero. Se midieron TRAb, TgAc y TPOAc séricos en 9 pacientes y en todos resultaron negativos. Entre los ocho pacientes con tirotoxicosis manifiesta en los que se realizó una ecografía tiroidea, se informaron signos de inflamación tiroidea en dos casos, pequeños nódulos tiroideos en otros tres pacientes, mientras que los tres pacientes restantes no mostraron ninguna alteración significativa de la estructura tiroidea. La tirotoxicosis manifiesta se acompañó de fibrilación auricular con frecuencia cardíaca alta en diez pacientes (32,3%). Además, cinco pacientes con tirotoxicosis manifiesta desarrollaron eventos tromboembólicos (accidente cerebrovascular isquémico en dos casos, tromboembolismo venoso en tres casos). Los médicos no registraron signos o síntomas locales de tiroiditis subaguda.
De los pacientes con tirotoxicosis manifiesta, 4 fueron tratados con tiamazol (metimazol-5 mg por día en todos los casos), mientras que los 27 pacientes restantes no recibieron fármacos dirigidos a la tiroides. A un paciente se le suspendió el tiamazol después de 3 días debido al aumento de las enzimas hepáticas. Se dispuso de un seguimiento a corto plazo en siete pacientes (dos tratados con tiamazol y cinco sin tratamiento) que mostraron una reducción en los valores de FT4 sérico independientemente del tratamiento de la tirotoxicosis.
Los valores de TSH sérica se correlacionaron inversamente con la edad. Pacientes con TSH por debajo 0,34 mU/L eran significativamente mayores en comparación con aquellos con TSH más altas, sin diferencias significativas entre <0,10 y 0,10–0,33 mU/L. Se midió la IL-6 sérica en 210 pacientes y resultó estar correlacionada significativamente con los valores de TSH y la edad. Los valores séricos de IL-6 fueron significativamente más altos en pacientes con TSH <0,34 mU/L en comparación con aquellos con valores más altos de TSH, sin diferencias significativas entre <0,10 y 0,1-0,33 mU/L.
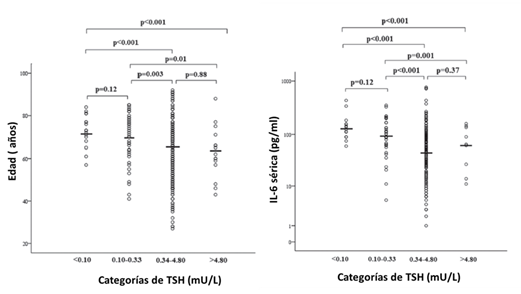
En el análisis de regresión logística multivariable, la tirotoxicosis resultó estar significativamente asociada con una IL-6 más alta (OR: 3,25, IC del 95%: 1,97–5,36; P < 0,001) pero no con la edad de los pacientes (OR: 1,03; IC del 95%: 0,99–1,06; P = 0,09).
Hubo un total de 60 muertes intrahospitalarias, correspondientes a una tasa de mortalidad intrahospitalaria del 21,4% entre los casos cerrados (n = 280). La mortalidad intrahospitalaria fue significativamente menor en pacientes con valores de TSH en el rango de referencia en comparación con aquellos con tirotoxicosis o hipotiroidismo. En los pacientes dados de alta, la duración de la hospitalización resultó ser significativamente más larga en los casos con tirotoxicosis en comparación con aquellos con TSH normal o hipotiroidismo
Este estudio retrospectivo informó, por primera vez, una alta prevalencia de tirotoxicosis manifiesta y subclínica en pacientes con COVID-19, en estrecha relación con niveles elevados de IL-6 circulante. Es de destacar que la prevalencia de hipotiroidismo fue baja en este contexto clínico y la mayoría de los casos fueron leves.
La rentabilidad y el valor diagnóstico de la medición de TSH sérica en pacientes hospitalizados son controversiales. De hecho, durante la enfermedad crítica se produce una importante alteración del eje hipotalámico-pituitario-tiroideo, el llamado “Eutiroideo Enfermo” (NTI) que se caracteriza por valores constantemente bajos de FT3 como consecuencia de una mayor desyodación de T4 en T3 reversa. Con el aumento de la gravedad de la enfermedad, se pueden observar niveles bajos de FT4 total y, a veces, niveles bajos de TSH. Un número notable de los pacientes de este estudio tuvo los valores suprimidos de TSH y este hallazgo fue muy probablemente una expresión de tirotoxicosis y no de NTI. De hecho, ninguno de estos pacientes tenía valores bajos de FT3 y en más de la mitad de ellos, los valores de FT4 estaban por encima del rango de referencia. Sin embargo, no se puede excluir que una posible NTI coexistente pueda haber influido en la presentación bioquímica de la tirotoxicosis, ya que la FT3 sérica aumentó menos que la FT4, no se encontraron diferencias significativas en los valores de FT3 entre la disfunción tiroidea manifiesta y subclínica, y la recuperación de la tirotoxicosis fue aparentemente más rápida que el observado en pacientes no hospitalizados. En este contexto, se puede hipotetizar el papel de IL-6, disminuyendo la secreción de T3 y posiblemente contribuyendo a los niveles normales de FT3 en los pacientes tirotoxicóticos.
Se encontró tirotoxicosis en aproximadamente el 20% de los pacientes y algunos otros mostraron TSH sérica en la parte inferior del rango de referencia. Estos hallazgos sugieren que COVID-19 puede favorecer el desarrollo de tirotoxicosis con una incidencia mayor que la esperada en la población general. Aunque este estudio no fue diseñado para esclarecer los mecanismos responsables de la disfunción tiroidea en pacientes con COVID-19, es razonable suponer que la tirotoxicosis fue causada por tiroiditis destructiva. Esta hipótesis fue apoyada por los hallazgos de que la tirotoxicosis fue a menudo leve y mejoró espontáneamente durante el seguimiento. Otro hallazgo que apoya este diagnóstico fue la negatividad para TRAb en los pocos pacientes en los que se evaluaron estos anticuerpos, aunque la ausencia de TRAb circulante no necesariamente excluye un hipertiroidismo leve similar a la Enfermedad de Graves. La estrecha relación entre la tirotoxicosis y la IL-6 sérica más alta en nuestros pacientes sugiere que la inflamación de la glándula tiroides podría ser provocada y sostenida por la tormenta de citokinas asociada con COVID-19, imitando los trastornos tiroideos que se desarrollan durante el curso de las inmunoterapias. Una hipótesis alternativa es la posible acción directa del SARS-CoV-2 sobre la glándula tiroides, basada en la evidencia de que varios tejidos y órganos pueden resultar directamente dañados por el virus. De hecho, existen pruebas de que el tejido tiroideo expresa en gran medida la enzima convertidora de angiotensina 2, la proteína utilizada por el SARS-CoV-2 para invadir células humanas.
Además de los aspectos fisiopatológicos, este estudio destaca algunos aspectos clínicos específicos sobre la relevancia clínica y el manejo de la tirotoxicosis en pacientes con COVID-19. El 16% de los pacientes con tirotoxicosis manifiesta desarrollaron eventos tromboembólicos, una tasa más de dos veces mayor que la reportada en pacientes COVID-19 hospitalizados en unidades de cuidados no intensivos. Este hallazgo, junto con la alta prevalencia de fibrilación auricular y la estrecha relación entre TSH suprimida y alta tasa de mortalidad así como una hospitalización más prolongada, sugieren que la tirotoxicosis puede ser clínicamente relevante en pacientes con COVID-19.
Como los pacientes estaban aislados, no se permitió la gammagrafía tiroidea y la evaluación ecográfica de la glándula tiroides se realizó solo en unos pocos casos. Por tanto, el enfoque terapéutico en estos pacientes fue empírico y bastante limitado. El tiamazol (metimazol) se utilizó en muy pocos pacientes basándose en la hipótesis de que la tirotoxicosis fue causada por tiroiditis destructiva en la que no se requiere una terapia específica más allá del tratamiento sintomático cuando está indicado. Si bien en algunos casos pudiera estar justificado el uso de corticoides con el fin de acelerar la resolución de la disfunción tiroidea, no se utilizaron debido al posible deterioro de la infección subyacente del SARS-CoV-2. Por tanto, la mayoría de los pacientes fueron seguidos sin tratamiento específico de la tirotoxicosis y la función tiroidea mejoró de forma espontánea. Cabe destacar que la tirotoxicosis puede favorecer el desarrollo de arritmias fatales en presencia de intervalo QT prolongado, un evento común en COVID-19, como efecto de terapias y/o trastornos electrolíticos. Por otro lado, la prevención y el tratamiento de los trastornos cardíacos relacionados con la tirotoxicosis pueden ser un desafío en el contexto de COVID-19, ya que algunos medicamentos utilizados para contrarrestar los efectos negativos de las hormonas tiroideas en el corazón (p. Ej., betabloqueantes) deben administrarse con precaución en pacientes con alteraciones preexistentes del ritmo cardíaco.
Este estudio tiene limitaciones. La falta de una cohorte independiente de pacientes con neumonía no permitió definir el verdadero impacto de COVID-19 en la función tiroidea y el riesgo de tirotoxicosis en este entorno clínico. En varios pacientes, se evaluó la función tiroidea durante el tratamiento con heparina de bajo peso molecular para la prevención de las complicaciones tromboembólicas venosas y arteriales de COVID-19. Se podría argumentar que el uso de heparina podría haber favorecido la elevación de FT4 en estos pacientes como efecto del desplazamiento de la hormona tiroidea de las proteínas transportadoras. Sin embargo, los valores de TSH suprimidos asociados con FT4 alto fueron altamente sugestivos de tirotoxicosis verdadera en lugar de una interferencia de drogas. El diseño retrospectivo, junto con el tamaño relativamente pequeño del grupo de estudio, impidió investigar el impacto independiente de la tirotoxicosis en el resultado de COVID-19. Además, no se permitió investigar si la función tiroidea podría verse influenciada por las inmunoterapias utilizadas en COVID-19. Por último, este estudio no aclaró si la tiroiditis crónica puede desarrollarse después de la resolución de COVID-19.
En conclusión, este estudio retrospectivo proporciona la primera evidencia de alto riesgo de tirotoxicosis después de la infección por SARS-CoV-2. Los estudios prospectivos futuros aclararán la relevancia clínica y pronóstico de la tirotoxicosis en pacientes con COVID-19.
Copyright 2020. Endoweb.net

Comentarios (-)
Todavía no hay comentarios en este artículo. ¡Nos encantaría conocer tu opinión!